Asetilasyon
Asetilasyon (veya IUPAC adlandırma sistemi ile etanoylasyon), organik bir bileşiğe bir asetil fonksiyonel grubu eklenme tepkimesidir. Deasetilasyon ise asetil grubunun çıkartılmasıdır.
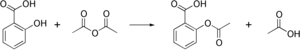
Bir diğer deyişle, asetilasyon bir bileşiğe bir asetil grubu eklenmesi, yani bir hidrojen grubu yerine bir asetil grubunun substitusyonudur. Bunun sonucundan bir asetoksi grubu meydana gelir. Bir hidroksit grubundaki hidrojen yerine bir asetil grubunun (CH3CO) gelmesi bir ester tipi olan asetatı meydana getirir. Asetik anhidrit serbest hidroksil grupları ile tepkimek için kullanılan yaygın kullanılan bir asetilasyon reaktifidir. Örneğin aspirin sentezinde kullanılır.
Proteinlerin asetilasyonu
Hücrelerde asetilasyon hem çevrimle eşzamanlı hem de çevrim sonrası bir değişim olarak meydana gelir. Asetilasyona uğrayan proteinler arasında histonlar, p53, ve tübülin sayılabilir.
N-alfa-uç asetilasyonu
Proteinlerin N-ucundaki alfa amin grubunun asetilasyonu ökaryotlarda çok yaygın görülen bir modifikasyondur. Maya proteinlerinin %40-50'si ve insan proteinlerinin %80-90'ı bu şekilde değişime uğrar, ve modifikasyonun şekli evrimsel olarak korunmuştur. Bu değişim N-alfa-asetiltransferazlar (NAT'lar) tarafından yapılır. NAT'lar, asetiltransferaz üst ailesi GNAT'ların bir alt ailesidir. GNAT'lar asetil-koenzim A'dan amin grubuna bir asetil grubu aktarırlar. NAT'lar en çok mayada çalışılmışlardır. Bu canlıda üç NAT kompleksi, NatA, B ve C çoğu N-alfa-uç asetilasyonunu gerçekleştirir. Substratlarının dizileri için spesifiteleri vardır. Bu enzimlerin ribozomlarla ilişkili olduğu, ve sentezlenen yeni peptitleri çevrim ile eşzamanlı olarak asetile ettikleri düşünülmektedir.
İnsanlarda, insan NatA ve NatB kompleksler tespit edilmiş ve karakterize edilmiştir. NatA kompleksinin altbirimlerinin kanserle ilişkili süreçlerde yer aldığı bulunmuştur: hipoksia tepkisi ve beta katenin yolu gibi. NatA'nın papiler tiroid karsinom ve nöroblastomada aşırı ifadesi gözlemlenmiştir. İnsan NatB kompleksi hücre döngüsü ile ilişkilidir. NatB kompleksinin Nat3 altbirimi bazı kanserlerde yüksek düzeyde ifade edilmektedir.
Korunmuş ve yaygın bir modifikasyon olmasına rağmen, N-alfa-uç asetilasyonunun biyolojik rolü bilinmemektedir. Aktin ve tropomiyosin proteinlerinin, düzgün aktin filamanları oluşturmak için NatB asetilasyonuna muhtaç oldukları bulunmuştur. Halen asetilasyonun biyolojik önemini gösteren başka örnekler bilinmemektedir.
Lizin asetilasyonu ve deasetilasyonu
Histon asetilasyonu ve deasetilasyonunda, histonlar N-uçlarındaki lizin kalıntılarında asetile ve deasetile olurlar, bu süreç gen düzenlemesi ile ilişkilidir. Tipik olarak bunu "histon asetiltransferaz" ve "histon deasetilaz" etkinliği olan enzimler yapar, ama bu enzimler histon olmayan proteinleri de modifiye edebilir.[1]
Transkripsiyon faktörleri, efektör proteinler, moleküler şaperonlar ve hücre iskeleti proteinlerinin asetilasyon / deasetilasyon yoluyla düzenlenmesi, çevrim sonrası değişim yoluyla gerçekleşen önemli mekanizmalardan biridir.[2] Bu bakımdan kinaz ve fosfatazlar tarafından gerçekleştirilen fosforilasyon ve defosforilasyon değişimlerine benzemektedir. Bir proteinin asetilasyon durumu onun etkinliğini belirlemektedir. Bu çevrim sonrası değişim, diğer değişimlerle (fosforilasyon, metilasyon, ubikuitinasyon, sumoylasyon, ve diğerleriyle) etkileşerek hücre sinyalizasyonunun dinamik kontrolüne sağlamaktadır.[3]
Tübülin asetilasyon ve deasetilasyon sistemi Chlamydomonas'da iyi anlaşılmıştır. Aksonemin ucunda yer alan bir tübülin asetiltransferaz, bütünleşmiş mikrotübülinde α-tübülin altbirimindeki belli bir lizin kalıntısını asetiller. Mikrotübülin ayrıştıktan sonra bu asetilasyon sitozolda bulunan spesifik bir deasetilaz tarafından çıkartılır. Bu iki enzimin etkinliklerinin sonucu, aksonemal mikrotübüllerdeki α-tübülin'in yarı ömrü uzun olması, sitozolik mikrotübüllerdekinin ise kısa ömürlü olmasıdır.
Kaynakça
- Sadoul K, Boyault C, Pabion M, Khochbin S (Şubat 2008). "Regulation of protein turnover by acetyltransferases and deacetylases". Biochimie. 90 (2). ss. 306-12. doi:10.1016/j.biochi.2007.06.009. PMID 17681659.
- Glozak MA, Sengupta N, Zhang X, Seto E (2005). "Acetylation and deacetylation of non-histone proteins". Gene. Cilt 363. ss. 15-23. doi:10.1016/j.gene.2005.09.010. PMID 16289629.
- Yang XJ, Seto E (2008). "Lysine acetylation: codified crosstalk with other posttranslational modifications". Mol Cell. Cilt 31. ss. 449-61. doi:10.1016/j.molcel.2008.07.002. PMID 18722172.
Ayrıca bakınız
- Asetoksi grubu
- Asilasyon
- Organik sentez