Potasyum ferrisiyanür
Potasyum ferrisiyanür K3[Fe(CN)6] formülü ile gösterilen inorganik bileşiktir. Bu parlak kırmızı tuz, oktahedral olarak koordine edilmiş [Fe(CN)6]3− iyonu içerir. Suda çözünür ve çözeltisi bir miktar yeşil-sarı flüoresans gösterir. 1822 yılında Leopold Gmelin tarafından keşfedilmiştir, ve başlangıçta ultramarin boyalarının üretiminde kullanılmıştır.
| Potasyum ferrisiyanür | |
|---|---|
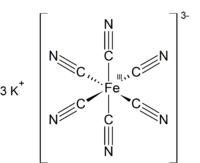 | |
potasyum hekzasiyanoferrat(III) | |
| Belirtilmiş yerler dışında verilmiş olan veriler, Standart sıcaklık ve basınçtadır. (25 °C, 100 kPa) | |
| Bilgi kutusu kaynakları |
Hazırlanması
Potasyum ferrisiyanür, klorun potasyum ferrosiyanür çözeltisinden geçirilmesiyle üretilir . Potasyum ferrisiyanür çözeltiden ayrılır:
- 2 K 4 [Fe(CN)6] + Cl 2 → 2 K3 [Fe(CN)6] + 2 KCl
Yapısı
Diğer metal siyanürler gibi, katı potasyum ferrisiyanür karmaşık bir polimerik yapıya sahiptir. Polimer, CN ligandlarına bağlı K + iyonları ile çapraz bağlanmış oktahedral [Fe(CN)6]3− merkezlerinden oluşur.[1] Katı madde suda çözündüğünde K + --- NCFe bağlantıları kopar.
Uygulamalar
Bileşik, plan çiziminde ve fotoğrafçılıkta (Siyanotip işlemi) yaygın olarak kullanılmaktadır. Birçok fotoğrafik baskı tonlama işlemi, potasyum ferrisiyanürün kullanımını içerir. Potasyum ferrisiyanür, ağartma olarak adlandırılan bir işlem olan gümüşü işlem sırasında renk negatiflerinden ve pozitiflerden çıkarmak için bir oksitleyici ajan olarak kullanıldı. Potasyum ferrisiyanür ağartıcılar çevre dostu olmayan olduğundan, demir kullanılarak ağartıcılar, kısa ömürlü, asit ile karıştırılır, eğer serbest hidrojen siyanür gazı sahip EDTA Kodak 1972 girmesinden bu yana renk işleme kullanılmıştır Cı-41 işlemi. Renk litografisinde, potasyum ferrisiyanür, nokta dağlama olarak adlandırılan bir tür manuel renk düzeltmesi olarak, sayıları azaltmadan renk noktalarının boyutunu azaltmak için kullanılır. Aynı zamanda, sodyum tiyosülfat (hipo) ile siyah beyaz fotoğrafta, karışımın Çiftçi redüktörü olarak bilinen negatif veya jelatin gümüş baskının yoğunluğunu azaltmak için kullanılır; bu, negatifin aşırı pozlanmasından kaynaklanan sorunları dengelemeye yardımcı olabilir veya baskıdaki vurguları aydınlatabilir.
Bileşik ayrıca demir ve çeliği sertleştirmede, elektrokaplamada, yün boyamada, laboratuvar reaktifi olarak ve organik kimyada hafif bir oksitleyici ajan olarak kullanılır.
Prusya mavisi
Prusya mavisi, baskıda derin mavi pigment, demir tuzları K3[Fe(CN)6] Fe(2+) demir iyonları gibi K4[Fe(CN)6] reaksiyonu ile oluşturulur.[2]
Histolojide, biyolojik dokudaki demir demiri tespit etmek için potasyum ferrisiyanür kullanılır. Potasyum ferrisiyaniür, genellikle Turnbull mavisi veya Prusya mavisi olarak adlandırılan çözünmeyen mavi pigmenti üretmek için asidik çözelti içindeki demir demiri ile reaksiyona girer. Demir (Fe 3+ ) demiri tespit etmek için Perls Prusya mavi boyama yönteminde bunun yerine potasyum ferrosiyanür kullanılır.[3] Turnbull'un mavi reaksiyonunda oluşan malzeme ile Prusya mavi reaksiyonunda oluşan bileşik aynıdır.
Emniyet
Potasyum ferrisiyanür düşük toksisiteye sahiptir, ana tehlikesi gözler ve cilt için hafif tahriş edici olmasıdır. Bununla birlikte, çok kuvvetli asidik koşullar altında, denkleme göre, oldukça toksik hidrojen siyanür gazı oluşur:
- 6H + + [Fe (CN) 6 ] 3− → 6 HCN + Fe 3+ [4]
Hidroklorik asit ile reaksiyon aşağıdaki gibidir:
- 6 HCI + K3 [Fe(CN)6] → 6 HCN + FeCl3 + 3 KCI
Ayrıca bakınız
- Ferrisiyanür
- Ferrosiyanat
- Potasyum ferrosiyanür
Kaynakça
- Figgis, B.N.; Gerloch, M.; Mason, R. "The crystallography and paramagnetic anisotropy of potassium ferricyanide" Proceedings of the Royal Society of London, Series A: Mathematical and Physical Sciences 1969, vol. 309, p91-118. DOI:10.1098/rspa.1969.0031
- Karlin, Kenneth D., (Ed.) (1996). Progress in Inorganic Chemistry. Progress in Inorganic Chemistry. 45. doi:10.1002/9780470166468. ISBN 9780470166468.
- Freida L. Carson (1997). Histotechnology (İngilizce). Amer Society of Clinical. ISBN 978-0-89189-411-7.
- "Arşivlenmiş kopya" (PDF). 18 Nisan 2016 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 17 Ocak 2020.