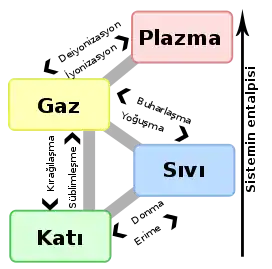
Uçuculuk
Kimyada, uçuculuk bir maddenin ne kolaylıkta buharlaştığını tanımlayan bir özelliktir. Belirli bir sıcaklık ve basınçta, yüksek uçuculuğa sahip bir maddenin buhar olarak bulunma olasılığı daha yüksekken, düşük uçuculuğa sahip bir maddenin sıvı ya da katı olma olasılığı daha yüksektir. Uçuculuk, bir buharın sıvı veya katı haline yoğunlaşma eğilimini de tarif edebilir; daha az uçucu madde, yüksek uçucu maddelere göre buhardan daha kolay yoğunlaşacaktır.[1] Uçuculuktaki farklılıklar, bir madde grubunun atmosfere açık olduğunda ne kadar hızlı buharlaştığını (veya katıysa süblimleştiğini) karşılaştırarak görülebilir. İspirto (izopropil alkol) gibi yüksek derecede uçucu bir madde hızlı bir şekilde buharlaşırken, bitkisel yağ gibi düşük uçuculuğa sahip bir madde yoğuşmuş kalacaktır.[2] Genel olarak, katılar sıvılardan daha az uçucudur, ancak bazı istisnalar da vardır. Kuru buz (katı karbondioksit ) veya iyot gibi süblimleşen (katıdan doğrudan buhara dönüşen) katı maddeler standart koşullar altında bazı sıvılarla aynı oranda buharlaşabilir.[3]

Tanım
Uçuculuğun kendisinin tanımlanmış bir sayısal değeri yoktur, ancak genellikle buhar basınçları veya kaynama noktaları (sıvılar için) kullanılarak tanımlanır. Yüksek buhar basınçları yüksek uçuculuk gösterirken, yüksek kaynama noktaları düşük uçuculuk gösterir. Buhar basınçları ve kaynama noktaları, ilgilenilen kimyasal maddeleri karşılaştırmak için kullanılabilecek tablo ve çizelgelerde sunulmaktadır. Uçuculuk verileri tipik olarak bir dizi sıcaklık ve basınç üzerinde yapılan deneylerde bulunur.
Buhar basıncı

Buhar basıncı, yoğunlaştırılmış bir fazın verilen bir sıcaklıkta nasıl buhar oluşturduğunun bir ölçüsüdür. Başlangıçta vakum altında (içinde hava olmadan) bulunan kapalı bir kaba konulan bir madde, boş bir alanı buharla hızla dolduracaktır. Sistem dengeye ulaştıktan sonra, daha fazla buhar oluşmadığında, bu buhar basıncı ölçülebilir. Sıcaklığın arttırılması, oluşan buhar miktarını ve dolayısıyla buhar basıncını arttırır. Bir karışımda, her bir madde karışımın genel buhar basıncına katkıda bulunur, uçucu bileşikler daha büyük katkı yapar.
Kaynama noktası
Kaynama noktası, bir sıvının buhar basıncının çevre basıncına eşit olduğu ve sıvının hızlı bir şekilde buharlaşmasına veya kaynamasına neden olan sıcaklıktır. Buhar basıncı ile yakından ilgilidir, ancak basınca bağlıdır. Normal kaynama noktası, atmosferik basınçtaki kaynama noktasıdır, ancak daha yüksek ve düşük basınçlarda da gözlemlenebilir.[1]
Etki eden faktörler
Moleküller arası kuvvetler
Bir maddenin uçuculuğunu etkileyen önemli bir faktör, molekülleri arasındaki etkileşimlerin gücüdür. Moleküller arasındaki çekici kuvvetler, malzemeleri bir arada tutar ve çoğu katı gibi moleküller arası kuvvetlere sahip malzemeler tipik olarak çok uçucu değildir. Etanol ve dimetil eter, aynı formüle sahip iki kimyasal (C2H6O) olmasına rağmen molekülleri arasında meydana gelen farklı etkileşimler sebebiyle sıvı fazında farklı uçuculuklara sahiplerdir: etanol molekülleri hidrojen bağı yapabilirken dimetil eter molekülleri yapamaz.[4] Sonuç olarak, etanol molekülleri arasında genel olarak daha güçlü bir çekici kuvvet elde edilir, bu da ikisinin daha az uçucu maddesi olmasını sağlar.
Moleküler ağırlık
Maddenin yapısı ve polaritesi gibi diğer faktörler uçuculukta önemli bir rol oynasa da, genel olarak uçuculuk artan moleküler kütle ile azalma eğilimindedir. Moleküler kütlenin etkisi, benzer yapıdaki kimyasalların (yani esterler, alkanlar, vs.) karşılaştırılmasıyla kısmen izole edilebilir). Örneğin, doğrusal alkanlar, zincirdeki karbon sayısı arttıkça uçuculuğu azaltır.
Uygulamalar
Damıtma
Uçuculuk bilgisi, bileşenlerin bir karışımdan ayrılmasında genellikle kullanışlıdır. Farklı uçuculuk seviyelerine sahip çok sayıda madde içeren yoğunlaşmış bir karışım, sıcaklığı ve basıncı değiştirerek ayrıştırılabilir. Daha az uçucu maddeler sıvı veya katı fazda kalırken, daha uçucu bileşenlerin buhara dönüşür ve toplanır. Yeni oluşturulan buhar daha sonra atılabilir veya ayrı bir kapta yoğunlaştırılabilir. Buharlar toplandığında, bu işlem damıtma olarak bilinir.[5]
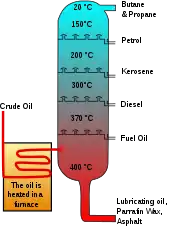
Petrolün rafine edilmesi işleminde, değişken uçuculuğa sahip çeşitli kimyasalların tek bir adımda ayrılmasını sağlayan, fraksiyonel damıtma olarak bilinen bir teknik kullanır. Rafineriye giren ham petrol, ayrılması gereken faydalı kimyasal maddelerden oluşur. Ham yağ bir damıtma kulesine akar ve ısıtılır, bu da bütan ve kerosen gibi daha uçucu bileşenlerin buharlaşmasını sağlar. Bu buharlar kuleyi yukarı doğru hareket ettirir ve sonunda soğuk yüzeylerle temas eder ve bu da yoğunlaşmalarına ve toplanmalarına neden olur. En uçucu kimyasallar sütunun en üstünde yoğunlaşırken en az uçucu kimyasallar en düşük kısımda yoğunlaşarak buharlaşır.[1]
Su ve etanol arasındaki uçuculuk farkı geleneksel olarak içilebilir alkolün rafine edilmesinde kullanılmıştır. Üründeki etanol konsantrasyonunu artırmak için, alkol yapıcılar, başlangıçtaki alkol karışımını, etanolün çoğunun buharlaştığı bir sıcaklığa kadar ısıtırken, suyun çoğu sıvı kalır. Etanol buharı daha sonra toplanır ve ayrı bir kapta yoğunlaştırılır, bu da daha konsantre bir ürün elde edilmesini sağlar.[6]
Parfüm
Uçuculuk parfüm üretirken önemli bir husustur. Aromatik buharlar burun içindeki reseptörlerle temas ettiğinde insanlar koku tespit eder. Uygulandıktan sonra hızla buharlaşan bileşenler, yağlar buharlaşmadan önce kısa bir süre için hoş kokulu buharlar üretecektir. Yavaş buharlaşan bileşenler cilt üzerinde haftalarca hatta aylarca kalabilir, ancak güçlü bir aroma üretmek için yeterli buhar üretmeyebilir. Bu sorunları önlemek için, parfüm tasarımcıları, esansiyel yağların ve diğer bileşenlerin parfümlerindeki uçuculuğu dikkatle değerlendirir. Uygun buharlaşma oranları, kullanılan yüksek uçucu ve uçucu olmayan bileşenlerin miktarının değiştirilmesiyle elde edilir.[7]
Ayrıca bakınız
- Clausius-Clapeyron ilişkisi
- Damıtma
- Kademeli damıtma
- Kısmi basıncı
- Raoult kanunu
- Bağıl uçuculuk
- Buhar-sıvı dengesi
- Uçucu organik bileşik
Kaynakça
- Felder, Richard (2015). Elementary Principles of Chemical Processes. John Wiley & Sons. pp. 279–281. ISBN 978-1-119-17764-7
- Koretsky, Milo D. (2013). Engineering and Chemical Thermodynamics. John Wiley & Sons. pp. 639–641.
- Zumdahl, Steven S. (2007). Chemistry. Houghton Mifflin. pp. 460–466. ISBN 978-0-618-52844-8.
- Atkins, Peter (2013). Chemical Principles. New York: W.H. Freeman and Company. pp. 368–369. ISBN 978-1-319-07903-1.
- Armarego, Wilfred L. F. (2009). Purification of Laboratory Chemicals. Elsevier. pp. 9–12. ISBN 978-1-85617-567-8.
- Kvaalen, Eric. "Alcohol Distillation: Basic Principles, Equipment, Performance Relationships, and Safety". Purdue.
- Sell, Charles (2006). The Chemistry of Fragrances. UK: The Royal Society of Chemistry. pp. 200–202. ISBN 978-0-85404-824-3.