Magnezyum nitrat
Magnezyum nitrat Mg(NO3)2(H2O)x formülüne sahip inorganik bileşikleri ifade eder. Formüldeki, x = 6, 2 ve 0 olabilir. Hepsi beyaz renkli katılardır.[2] Susuz madde higroskopiktir, havada bekletildiğinde hızlı bir şekilde hekzahidrat oluşturur. Bütün tuzları hem suda hem de etanolde çok çözünür.
| Magnezyum nitrat | |
|---|---|
 | |
 | |
Magnezyum nitrat | |
Diğer adlar Nitromagnezit (hekzahidrat) | |
| Tanımlayıcılar | |
| CAS numarası | 10377-60-3 |
| PubChem | 25212 |
| EC numarası | 233-826-7 |
| UN numarası | 1474 |
| ChEBI | 64736 |
| RTECS numarası | OM3750000 (susuz) OM3756000 (hekzahidrat) |
| SMILES |
|
| InChI |
|
| ChemSpider | 23415 |
| Özellikler | |
| Molekül formülü | Mg(NO3)2 |
| Molekül kütlesi | 148.32 g/mol (susuz) 184.35 g/mol (dihidrat) 256.41 g/mol (hekzahidrat) |
| Görünüm | Beyaz kristal katı |
| Yoğunluk | 2.3 g/cm3 (susuz) 2.0256 g/cm3 (dihidrat) 1.464 g/cm3 (hekzahidrat) |
| Erime noktası |
129 °C ((dihidrat) |
| Kaynama noktası |
330 °C (bozunur) |
| Çözünürlük (su içinde) | 71 g/100 mL (25 ºC)[1] |
| Çözünürlük () | etanol ve amonyakta kısmen çözünür |
| Termokimya | |
Standart formasyon entalpisi (ΔfH |
-790.7 kJ/mol |
Gibbs serbest enerjisi (ΔfG˚) |
-589.4 kJ/mol |
| Tehlikeler | |
| GHS piktogramları |   |
| GHS İşaret sözcüğü | Tehlike |
| R-ibareleri | R8, R36, R37, R38 |
| G-ibareleri | S17, S26, S36 |
| H-ibareleri | H272 |
| P-ibareleri | P210, P220, P280, P370+378, P501 |
| NFPA 704 |
 0
1
0
|
| Parlama noktası | Yanıcı değildir |
| LD50 | 5440 mg/kg (sıçan, oral) |
| Benzeyen bileşikler | |
Diğer anyonlar |
Magnezyum sülfat Magnezyum klorür |
Diğer katyonlar |
Berilyum nitrat Kalsiyum nitrat Stronsiyum nitrat Baryum nitrat |
| Belirtilmiş yerler dışında verilmiş olan veriler, Standart sıcaklık ve basınçtadır. (25 °C, 100 kPa) | |
| Bilgi kutusu kaynakları | |
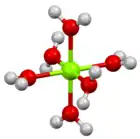
Oluşumu, hazırlanması, yapısı
Suda çözünürlüğü yüksek olan magnezyum nitrat, doğal olarak sadece madenlerde ve mağaralarda nitromagnezit (hekzahidrat form) olarak bulunur.[3]
Ticarette kullanılan magnezyum nitrat, nitrik asit ve çeşitli magnezyum tuzlarının reaksiyonu ile yapılır.
Kullanımı
Başlıca olarak, derişik nitrik asitin hazırlanmasında bir dehidrasyon maddesi olarak kullanılır.[2]
Gübre olarak, %10.5 azot ve %9.4 magnezyum içerir. Bu nedenle, 10.5-0-0 + %9.4 Mg olarak listelenir. Magnezyum nitrat içeren gübre karışımları ayrıca, çoğunlukla amonyum nitrat, kalsiyum nitrat, potasyum nitrat ve mikro besinlere sahiptir. Bu karışımlar sera ve hidroponik uygulamalarında kullanılır.
Reaksiyonları
Magnezyum nitrat, ilgili nitratı oluşturmak için alkali metal hidroksit ile reaksiyona girer:
- Mg(NO3)2 + 2 NaOH → Mg(OH)2 + 2 NaNO3.
Magnezyum nitratın su ile birleşme eğilimi yüksek olduğundan hekzahidratın ısıtılması, tuzun dehidrasyonuna değil, bunun yerine magnezyum oksit, oksijen ve azot oksitlere ayrışmasına neden olur:
- 2 Mg(NO3)2 → 2 MgO + 4 NO2 + O2.
Bu azot oksitlerin su içinde soğurulması, nitrik asiti sentezlemek için olası bir yoldur. Verimsiz olmasına rağmen, bu yöntem kuvvetli asit kullanılmasını gerektirmez.
Aynı zamanda kurutucu olarak da kullanılır.
Kaynakça
- Şablon:RubberBible87th
- Thiemann, Michael; Scheibler, Erich and Wiegand, Karl Wilhelm (2005). "Nitrik Asit, Nitröz Asit veAzot Oksitler". Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a17_293.
- Mindat, http://www.mindat.org/min-2920.html 5 Haziran 2020 tarihinde Wayback Machine sitesinde arşivlendi.
- Schefer, J.; Grube, M. (1995). "Low temperature structure of magnesium nitrate hexahydrate, Mg (N O3)2 . 6(H2 O): a neutron diffraction study at 173 K". Materials Research Bulletin. 30: 1235-1241. doi:10.1016/0025-5408(95)00122-0.
Dış bağlantılar
- Sıvı Kimyası
- Nitromagnezit Mineral Verisi19 Ekim 2011 tarihinde Wayback Machine sitesinde arşivlendi.
- Magnezyum Nitrat MSDS4 Şubat 2012 tarihinde Wayback Machine sitesinde arşivlendi.