Kalsiyum oksit
Kalsiyum oksit (CaO) ya da sönmemiş kireç geniş bir kullanım alanı bulunan bir çeşit kimyasal bileşiktir. Beyaz renkli,aşındırıcı ve alkalik bir katıdır. Sanayide kireç taşlarını yüksek sıcaklıklarda eriterek karbondioksidin uzaklaştırılmasıyla elde edilir. Suyla reaksiyona girerse oksitlenir ve kalsiyum hidroksidi oluşturur.
| Kalsiyum oksit | |
|---|---|
 | |
 | |
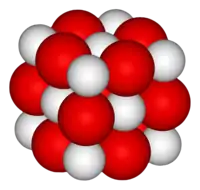
Kalsiyum oksit | |
Diğer adlar sönmemiş kireç, yanmış kireç | |
| Tanımlayıcılar | |
| CAS numarası | 1305-78-8 |
| PubChem | 14778 |
| UN numarası | 1910 |
| RTECS numarası | EW3100000 |
| ATC kodu | P53 |
| SMILES |
|
| InChI |
|
| ChemSpider | 14095 |
| Özellikler | |
| Molekül formülü | CaO |
| Molekül kütlesi | 56.0774 gr/mol |
| Görünüm | Beyazdan sarı/kahverengiye kadar değişen renklerde toz |
| Koku | kokusuz |
| Yoğunluk | 3.34 gr/cm³[1] |
| Erime noktası |
2613 °C |
| Kaynama noktası |
3850 °C ((100 hPa)[2]) |
| Çözünürlük (su içinde) | tepkime vererek kalsiyum hidroksit şekline döner |
| Çözünürlük (metanol içinde) | (ayrıca dietil eter, n-oktanolde) çözünmez |
| Asitlik (pKa) | 12.8 |
| Termokimya | |
Standart formasyon entalpisi (ΔfH |
−635 kJ•mol−1[3] |
| Tehlikeler | |
| GHS piktogramları |   |
| GHS İşaret sözcüğü | Tehlike |
| NFPA 704 |
 0
3
2
|
| Parlama noktası | Yanıcı değildir |
| ABD maruz kalma limiti (PEL) |
TWA 5 mg/m³[4] |
| Benzeyen bileşikler | |
Diğer anyonlar |
Kalsiyum sülfit Kalsiyum hidroksit Kalsiyum selenit Kalsiyum tellürit |
Diğer katyonlar |
Berilyum oksit Magnezyum oksit Stronsiyum oksit Baryum oksit Radyum oksit |
| Belirtilmiş yerler dışında verilmiş olan veriler, Standart sıcaklık ve basınçtadır. (25 °C, 100 kPa) | |
| Bilgi kutusu kaynakları | |
Formülü CaO ve iyonik bağlı bir bileşiktir. Bazik özellik gösterir.
Kaynakça
- Calciumoxid 30 Aralık 2013 tarihinde Wayback Machine sitesinde arşivlendi.. GESTIS database
- Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. s. A21. ISBN 0-618-94690-X.
- "NIOSH Pocket Guide to Chemical Hazards #0093". National Institute for Occupational Safety and Health (NIOSH).
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.