Tiyokarbonik asit
Tiyokarbonik asit, karbonik asit ile ilişkili bir inorganik asittir. Kimyasal formülü H2CS3 olan kararsız kırmızı bir yağdır. Diğer tiyokarbonatlardan ayırt etmek için sıklıkla tritiyokarbonik asit olarak adlandırılır.
| Tiyokarbonik asit | |
|---|---|
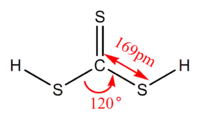 | |
karbonotritiyoik asit | |
Diğer adlar tritiyokarbonik asit | |
| Tanımlayıcılar | |
| CAS numarası | 594-08-1 |
| PubChem | 68982 |
| EC-numarası | 209-822-6 |
| ChEBI | CHEBI:36967 |
| SMILES |
|
| ChemSpider | 62204 |
| Özellikler | |
| Molekül formülü | CH2S3 |
| Molekül kütlesi | 110.22 g/mol |
| Görünüm | kırmızı, yağlı sıvı |
| Yoğunluk | 1.483 g/cm3(sıvı) |
| Erime noktası |
−26.8 °C (−16.3 °F) |
| Kaynama noktası |
58 °C (136 °F) |
| Belirtilmiş yerler dışında verilmiş olan veriler, Standart sıcaklık ve basınçtadır. (25 °C, 100 kPa) | |
| Bilgi kutusu kaynakları | |
Keşif ve sentezi
İlk olarak 1824'te Zeise tarafından kısaca ve daha sonra 1826'da Berzelius tarafından daha ayrıntılı olarak rapor edildi,[1] her iki durumda da karbon disülfürün bir hidrosülfür tuzu (örn. Potasyum hidrosülfür) üzerindeki etkisi ile üretildi.[2]
- CS2 + 2 KSH → K2CS3 + H2S
Asitlerle muamele, tiyokarbonik asidi kırmızı bir yağ halinde serbest bırakır.
- K2CS3 + 2 HX → H2CS3 + 2 KX
Hem asit hem de tuzlarının birçoğu kararsızdır ve özellikle ısıtma üzerine karbon disülfür salınımı yoluyla ayrışır:
- H2CS3 → CS2 + H2S
Uygulama
Tiyokarbonik asidin şu anda önemli bir uygulaması yoktur. Bazen tioksantat olarak adlandırılan esterler RAFT polimerizasyonunda kullanım bulur.
Kaynakça
- Berzelius, J. J. (1826). "Ueber die Schwefelsalze" [About the sulfur salts]. Annalen der Physik (in German). 82 (4): 425–458. doi:10.1002/andp.18260820404.
- O'Donoghue, Ida Guinevere; Kahan, Zelda (1906). "CLXXIV.—Thiocarbonic acid and some of its salts" (PDF). J. Chem. Soc., Trans. 89 (0): 1812–1818. doi:10.1039/CT9068901812.