Kütle spektrometrisi
Kütle spektrometrisi, İngilizce: Mass spectrometry (MS), kimyasal türleri iyonize edip oluşan iyonları kütle/yük oranını esas alarak sıralayan bir analitik teknik. Daha basit terimler ile, bir kütle spektrumu bir numunen içindeki kütleleri ölçer. Kütle spektrometrisi birçok farklı alanda kullanılır ve kompleks karışımlara uygulandığı kadar saf numunelere de uygulanır.

Bir kütle spektrumu, kütle/yük oranının bir fonsiyonu olan iyon sinyallerinin grafiğidir. Bu spektrumlar, bir numunenin elementsel veya izotopik imzaları, parçacıkların ve moleküllerin kütlerlerini belirlemek ve moleküllerin kimyasal yapılarını orataya çıkarmak için kullanılır. Peptitlerin ve diğer kimyasal bileşiklerin kimyasal yapıları kütle spektrometresi ile ortaya çıkartılabilir.
Tipik bir MS prosedüründe, katı, sıvı veya gaz olabilecek bir numune iyonlaştırılır, bu işlem numuneye elektron bombardımanı ile yapılabilir. Bu işlem bazı numune moleküllerinin yüklü parçalara ayrılmalarına sebebiyet verir. Sonrasında bu iyonlar kütle/yük oranına göre birbirinden ayrılırlar, bu ayrılma genellikle onları hızlandırıp bir lektrik veya manyetik alana maruz bırakarak başarılır. Aynı kütle/yük oranına sahip iyonlar aynı sapma hareketini yaşar.[1] İyonlar elektron multipleri gibi yüklü parçacıkları tanımlayabilen bir mekanizma tarafından tespit edilir. Sonuçlar kütle/yük oranının bir fonksiyonu olan belirlenen iyonların bağıl çokluğunun spektrumlar halinde görüntülenir. Numunedeki atomlar veya moleküller bilinen kütlelerin (bir bütün molekül gibi) cihaz tarafından tanımlanmış kütleler veya karakteristik bir parçalanma örneği ile bağdaştırılması ile tespit edilebilir.
Tarihi
.jpg.webp)
1886' da, Eugen Goldstein düşük basınçta gaz deşarjında, anottan uzaklaşıp delikli katotun içinden geçen, negatif yüklü- katottan anoda seyahat eden- katot ışınlarına ters yönde ışınlar gözlemlemiştir. Goldstein bu pozitif yüklü anod ışınlarına "Kanalstrahlen"; Türkçeye standart çevirisi ile "kanal ışınları" adını vermiştir. Wilhelm Wien güçlü elektrik veya manyetik alanın kanal ışınlarını saptırdığını buldu ve 1899'da elektrik ve manyetik alanların birbirine dik olduğu bir makine kurdu. Bu alanlar pozitif ışınların birbirlerinden kütle/yük oranına (Q/m) göre yarılmasını sağlıyordu. Wien aynı zamanda kütle/yük oranının gazların gaz deşarjın tübündeki doğalarına bağlı olduğunu fark etti. İngiliz bilimci J.J. Thomson Wien'in çalışmasını basıncı düşürerek geliştirerek kütle spektrografını oluşturdu.

Spectrograph kelimesi 1884' te uluslararası bilimsel kelime dağarcığının bir parçası oldu.[2][3] İlkel spektrometri cihazlarının, iyonların kütle/yük oranını ölçmüş olanları kütle spektrografları şeklinde adlandırlır. Bu cihazlar kütle değerlerinin spektrumlarını bir fotoğraf plakasına kaydeden aletlerden oluşur.[4][5] Kütle spektroskopu kütle spektrografına benzerdir. Fakat kütle spektroskopu ışık hüzmesinin bir fosfor ekranına yansıtılması işlemiye farklılık gösterir.[6] Kütle spektroskopu konfigürasyonu konfigürasyonu düzeltmelerin etkilerinin hızlıca gözlenmesi için kullanılırdı. Alet bir kere düzgünce ayarlandığında, bir fotografik tabak eklenir ve işleme mağruz bırakılırdı. Kütle spektroskopu terimi, osiloskop ile dolaylı yoldan ölçümün fosfor ekran ile gösterimin yerini almasına rağmen, hala kullanımı sürmektedir.[7] Kütle spektroskopisi teriminin kullanımı ışık spektroskopisi terimi ile karıştırılma olasılığından dolayı artık kullanılmamaktadır.[8] Kütle spektrometri ifadesi sıkça kütle-spek veya basitçe MS şeklinde kısaltılır.
Kütle spektrometrisinin modern teknikleri sırasıyla 1918 ve 1919' da Arthur Jeffrey Dempster ve F.W. Aston tarafından icat edilmiştir.
Sektör kütle spektrometreleri, kalutronlar olarak da bilinirler, Ernest O. Lawrence tarafından Manhattan Projesi boyunca uranyum izotoplarını ayırmak amacı ile geliştirilmiştir.[9] Kalutronlar Oak Ridge, Tennessee Y-12 tesisinde II. Dünya Savaşı sırasında kuruldu ve uranyum zenginleştirmeleri için kullanıldı.
1989'da, Nobel Fizik Ödülü 1950' ler ve 1960' larda geliştirdikleri iyon tuzağı tekniği sebebi ile Hans Dehmelt ve Wolfgang Paul'e verildi.
2002' de, Nobel Kimya Ödülü elektrosprey iyonizasyonunu (electrospray ionization, ESI) geliştirmesi sebebi ile John Bennett Fenn' e ve yumuşak lazer desorpsiyonu (soft laser desorption- SLD) icadı ile bu tekniğin biyolojik makromoleküller, özellikle proteinler, üzerine uygulanması üzerine yaptığı çalışmalardan dolayı Koichi Tanaka' ya verilmiştir.[10]
Kütle spektrometresinin parçaları
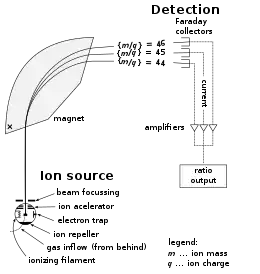
Bir kütle spektrometresi üç parçadan ibarettir: bir iyon kaynağı, bir kütle analizörü ve bir de detektör. İyonlaştırıcı numunenin bir kısmını iyonlara dönüştürür. Oldukça çeşitli iyonlaştırma tekniği mevcuttur, bunlar numunenin fazı (katı, sıvı, gaz) ve bilinmeyen türler için iyonlaştırma mekanizmasının verimi açısından farklar gösterir. Bir ekstraksiyon sistemi iyonları numun eden uzaklaştırır ardından iyonlar kütle analizörü ve ondan sonra detektöre ulaşır. Parçalar arasındaki kütle farkı, kütle analizörünün parçaları kütle/yük oranını temel alarak sıralamasına imkân sağlar. Detektör belirteç miktarın değerini ölçer ve ortamada bulunan her iyonun bulunma yüzdesini hesaplamak için veri sağlamış olur. Bazı detektörler (multikanal tabak gibi) aynı zamanda uzaysal bilgi sağlar.
Teoritik örnek
Takip eden örnek sektör tipi olan bir kütle spektrometre kütle analizörünün işlemini açıklamatadır. (Diğer analizör tipleri aşağıda ele alınmıştır.) Sodyum klorürü (sofra tuzu) düşünün. İyon kaynağında, numune buharlaştırılır (gaza dönüştürülür) ve sodyum (Na+) ve klorür (Cl−) iyonlarına iyonlaştırılır. Sodyum atomları ve iyonları 23 u civarında bir kütle ile monoizotopiklerdir. Klorür atom ve iyonları ise 2 izotopludur, yaklaşık 35 u (% 75 doğada bulunma yüzdesi) ve yaklaşık 37 u (% 25 doğada bulunma yüzdesi). Spektrometrenin analizör parçası içerisinden geçen iyonlara kuvvet uygulayan elektrik ve manyetik alanları içerir. Yüklü parçacığın hızı elektrik alan boyunca yükselebilir veya düşebilir ve hareket yönü manyetik alan tarafından hareket yönü değiştirilebilir. Hareket halindeki iyonun yörüngesinin sapmasının büyüklüğü, iyonun kütle/yük oranına bağlıdır. Hafif iyonlar manyetik alan tarafından ağır iyonlardan daha fazla saptırılırlar (ki Newton'un ikinci hareket yasasınca mantıklıdır, F = ma). Sıralanmış iyon sürüleri analizörden -her iyonun bağıl bulunma oranlarını kayıt eden-detektöre geçerler. Bu bilgi orijinal numunenin kimyasal element bileşiminin bulunmasında kullanılır. Sodyum klorür örneğine dönülecek olursa 35Cl/ 37Cl oranının bu bilgi ışığında tespiti sağlanmış olur.
İyonların oluşturulması

İyon kaynağı analiti (analiz işleminde bulunan materyal) iyonlaştıran kütle spektrometre parçası. Daha sonra iyonlar manyetik veya elektrik alandan kütle analizörüne aktarılır. İyonlaştırma amaçlı teknikler, ne tip numunelerin kütle spektrometrisi tarafından analiz edileceğinin belirlenmesinde kilit noktadır. Elektron iyonizasyonu ve kimyasal iyonizasyon gazlar ve buharlar için kullanılır. Kimyasal iyonizasyon kaynaklarında, analit, kaynaktaki çarpışamlardaki, kimyasal iyon-molekül tepkimeleri ile iyonlaşır. İki teknik biyolojik sıvı ve katılarda sıkça kulllanılır. Bu iki teknik elektrosprey iyonizasyon (John Fenn tarafından icat edimiştir[11]) ve matriks-destekli lazer desorpsiyon/iyonizasyondur (matrix-assisted laser desorption/ionization-MALDI). MALDI benzeri bir teknik olarak "Yumuşak Lazer Desorpsiyonu (Soft Laser Desorption-SLD)" adı ile K. Tanaka tarafından oluşturumuştur.[12] Tanaka bu buluşu sebebi ile M. Karas ve F. Hillenkamp (MALDI' nin mucitleri) ile beraber Nobel Ödülü ile ödüllendirilmiştir.[13].
Sert iyonizasyon ve yumuşak iyonizasyon

Kütle spektrometresinde, iyonizasyon kütle filtrelerinde veya kütle analizörlerinde çözürlük için uygun gaz faz iyonlarının üretilmesi anlamına gelir. İyonizasyon iyon kaynağında gerçekleşir. Birkaç iyon kaynağı seçeneği mevcuttur. Her biri farkı uygulama alanlarında farklı avantajlara ve dezavantajlara sahitir. Örneğin, Elektron iyonizasyonu (Electron ionization-EI) çok fazla parça oluşmasına sebep olur ve bu da çok ayrıntılı bir kütle spektrumuyla sonuçlanır. Bu tip ayrıntılı kütle spektrumlarının yetkin bir şekilde analizi yapısal izah ve karakterin belirlenmesi için önemli bilgiler sağlar. Aynı zamanda bu yetkin analiz, bilinmeyen bir bileşiğin kimliklendirlmesini, özdeş işlem koşulları altında elde edilmiş kütle spektral kütüphaneler ile karşılaştırmalar yapılmasına olanak sağlayarak, kolaylaştırır. Ancak, EI HPLC(Yüksek perfromans sıvı kromatografisi), ile kombine edilemez, yani LC-MS (Sıvı kromatografi-Kütle spektrometrisi) kombini oluşturulamaz. Çünkü atmosferik basınçta (HPLC' nin çalıştığı basınç), elektron oluşturmak için kullanılan filament (bu filament, kütle spektrometresi aletinin içinde düşük basınçta bulunur) hemen yanar. EI genellikle GC (gaz kromatografisi) ile kombine edilir, ve GC-MS (Gaz kromatografi-Kütle spektrometrisi) oluşmuş olur. Bu kombinde bütün sistem yüksek vakum altındadır, yani basınç oluşturabilecek bilelşenler vakum tarafından kullanılır ve sistem düşük basınç altında çalışır.
Sert iyonizasyon teknikleri hedef moleküler yüksek miktarda enerji vererek birçok parçacığın oluşmasına sebebiyet veren işlemlerdir. Parçacık oluşumunda bağlantıların sistematik kırılması fazla enerjinin atılmasını sağlayarak oluşan iyonun kararlı olmasını sağlar. Proton transferi ve izotop zirveleri vakaları haricinde oluşan iyonlar moleküler kütlelerinden daha düşükte bir m/z (kütle/yük) oranına sahip olma eğilimindedir. Sert iyonizasyonun en yaygın örneği elektron iyonizasyonudur (EI).
Yumuşak iyonizasyon hedef moleküle az enerji verilmesi ile daha az parçacığın oluşması işlemidir. Örnekleri:
İndüksiyonla birleşmiş plazma

İndüksiyonla birleşmiş plazma (Inductively Coupled Plasma-ICP) kaynakları,başlıca, fazlaca çeşitli olan bir dizi numune tiplerinin katyon analizleri için kullanılır. Bu kaynakta, elektriksel olarak yüksüz fakat yüksek sıcaklıkta yüksek oranda atomları iyonlaşan bir plazma kullanılır. Bu kullanımın amacı numune molekülü atomize etmek(atomlarına ayırmak) ve daha da ötesi oluşan atomların en dış katmanından elektron kopartmaktır. Plazma genel olarak Argon gazından üretilir. Bunun sebebi Argon atomlarının ilk iyonlaşma enerjisi He, O, F ve Ne' ninki hariç diğer atomlardan daha yüksektir fakat ikinci iyonlaşma enerjisi için bu durum "Ar atomlarının ikinci iyonlaşma enerjisi çoğu elektropozitif metalinki hariç diğer atomların ikinci iyonlaşma enerjisinden düşüktür" şeklinde ifade edilir. Isıtma plazmayı çevreleyen bir bobiniden bir radyo-frekansı akımının geçirilmesi ile başarılır.
Fotoiyonizasyon kütle spektrometrisi
Fotoiyonizasyon kütle spektrometrisini kimyasal kinetik mekanizmasını veya izometrik ürün dallanmasını çözme üzerine odaklanan deneylerde kullanılabilir.[14] Bu gibi durumlarda, yüksek enerjili foton, X-ışını ya da UV, kararlı gaz moleküllerini taşıyıcı gazdan(He veya Ar) ayırmak için kullanılır. Bir senkrotronun ışık kaynağı olarak kullanıldığı vakalarda, ayarlanabilir foton enerjisi fotoiyonizasyon verimlilik eğrisi elde etmek için kullanılabilir. Fotoiyonizasyon verimlilik eğrisi m/z oranını ile bağdaştırılarak kullanıldığında moleküler veya iyonik türlerin kütle spektrometri parmak izinin (yani hangi iyonik veya moleküler türün hangi m/z oranına denk geldiği bilgisi) elde edinilebilir.
Diğer iyonizasyon teknikleri
Alan desorpsiyonu (Field Desorption-FD)
Hızlı atom bombardımanı (Fast Atom Bombardment-FAB)
Termosprey
Silikon üzerinde desorpsiyon/iyonizasyon (Desorption/Ionization on Silicon-DIOS)
Gerçek zamanlı direkt analiz (Direct Analysis in Real Time-DART)
Atmosferik basınçta kimyasal iyonizasyon (Atmospheric Pressure Chemical Ionization-APCI)
İkincil iyon kütle spektrometrisi (Secondary Ion Mass Spectrometry-SIMS)
Kıvılcım iyonizasyon
Termal iyonizasyon (Thermal Ionization Mass Spectrometry-TIMS)[15]
Kütle analizi
Kütle analizörü iyonları m/z oranına göre ayırır. Takip eden iki yasa vakumdaki elektrik ve manyetik alanda yüklü parçacıkların dinamiklerini yönetir:
- (Lorentz kuvveti yasası);
- (Relavisitik olmayan durumda,diğer bir deyişle sadece iyon hızının ışığın hızından çok daha düşük olduğunda gerçerli olan, hareketin Newton'un ikinci yasası).
F=iyon üzerine uygulanan kuvvet m=iyonun kütlesi a= ivme Q=iyonun yükü E=elektrik alan v × B = iyon hızı ve manyetik alanın çapraz çarpım ürünü
Yukarkdaki iki denklemde kuvveti ifade etmektedir, yani denktirler :
Bu diferansiyel denklem yüklü parçacık hareketinin klasik denklemidir. Parçacığın önceki durumu ile beraber, bu denklem parçacığın uzadaki harekenin m/Q oranına göre tümüyle belirleyicisidir. Bundan dolayı kütle spektrometreleri "kütle/yük spektrometreleri" olarak düşünülebilir. Veri sunulurken, (resmi olarak) m/z' nin (z=iyon üzerindeki temel yük(e) sayısı, z=Q/e) boyutsuz olarak kullanımı yaygındır. Bu miktar (m/z), resmi olmyan bir şekilde kütle/yük oranı diye ifade edilse de, kesin olarak konuşulduğunda kütle numarası (z) ve yük numarasının (z) oranıdır.
Birçok tip kütle analizörü vardır. Statik veya dinamik alanların ve manyetik veya elektrik alanların hangisini kullandığı fark etse de farklı tip analizörlerin hepsi yukardaki diferansiyel denklem esasında çalışır. Her analizör tipi kendi güçlü ve zayıf yanlarını barındırır. Birçok kütle spektrometre ardışık kütle spektrometre (MS/MS) oluşturmak için iki veya daha fazla kütle analizörü kullanır. Aşağıda listelenmiş olan daha yaygın kütle analizörlerine ek olarak özel durumlara binaen tasarlanmış diğer türler vardır.
Birkaç önemli analizör özelliği vardır. Bunlar, kütle çöznürlük gücü, kütle kesinliği, kütle menzili, lineer dinamik menzili ve hız şeklinde sıralanır. Kütle çözünürlük gücü birbirinden farklı iki yakın m/z zirvenin birbirinden ayırt edilebilme ölçüsüdür. Kütle kesinliği ölçülen m/z ölçüm hatasının doğru m/z' ye oranıdır. Kütle menzili verilen analizöre uygun olarak analiz edilebilecek m/z aralığıdır. Lineer dinamik menzil iyon sinyalinin analit konsantrasyonu ile lineer olduğu aralıktır. Hız deneyin zaman çerçevesidir ve birim zamana düşen oluşturlabilecek spectra sayısının belirlenmesinde kullanılır.
Sektör enstrümanı

Bir sektör alan kütle analizörü yüklü parçacıkların hızını ve/veya yolunu etkilemek amacı ile bir statik elektrik ve/veya manyetik alan kullanır. Yukarıda gösterildiği üzere, sektör enstrümanı iyonlar kütle analizöründen geçerken onların rotalarını değiştirir. Bu işlemi m/z oranına göre yapar, daha çok yüklü ,hızlı ve hafif parçacıklar daha çok sapma gösterir. Bu analizör daha inçe menzil seçimleri için kullanılabilir veya bir aralığın içinde bulunan bütün m/z' leri tarayarak ortamda bulunan iyonların kataloğunu çıkartmak için kullanabilir.[16]
Uçuş süresi
Uçuş süresi (time-of-flight/TOF) analizörü aynı potansiyel ile iyonları bir elekrik alan kullanarak hızlandırır ve iyonların detektöre varma sürelerini ölçer. Eğer bütün parçalar aynı yüke sahip ise, kinetik enerjileri de aynı olma eğilimindedir ve bu durumda yionların hızları kütlelerine bağıl olarak değişir.[17] Ancak aynı m/z' ye sahip olanlar parçalar bile detektöre farklı zamanlarda varabilirler çünkü farklı ilk hızlara sahiptirlerdir. İyonun ilk hızı kütleye bağıl değildir, yani ilk hız kütleden bağımsızdır, bu da TOF-MS(TOF- kütle spektrometri) tekniğinin problemli noktasıdır. İlk hızlar arasındaki fark kendini son hızlarda da gösterir, ilk hızlardaki fark son hızlardaki farka dönüşür. Böylece, aynı m/z değerine sahip iyonlar detektöre farklı zamanlarda varmış olur. Bu problemin üzerinden gelebilmek için zaman-gecikmesi odaklı/ertelenmiş ekstraksiyon TOF-MS ile birleştirilir.[18]
Kuadrupol kütle filtresi
Kuadrupol kütle analizörleri, radyo frekansı(RF) kuadrupol alanının (kuadrupol alanı 4 paralel çubuk ile oluşturur) içinden geçen iyonların rotalarını titreşen elektrik alan kullanarak seçici olarak stabilize ve destabilize eder. alandan sadece belirli bir m/z aralığının içinde kalan parçalar girer ama çubuklardaki potansiyelin değiştirilmesiylem/z değerleri geniş bir aralığa hızlıca kaydırılabilir. Bu kaydırma işlemi tek bir hamlede kesiksiz veya kesikli (birden fazla hamlede) gerçekleştirilebilir. Bir kuadrupol kütle analizörü bir kütle seçici filtre gibi davranır ve Paul tuzağı, iyon tuzağı tuzaklanması hedeflenen parçaları değil de hedeflenmeyen parçaları tuzaklamak için tasarlanmış olması dışında özellikle de lineer kuadrupol iyon tuzağı, ile yakından ilişkilidir. Bu özelliğinden dolayı bu yapılar geçiş kuadrupolleri olarak da bilinirler. Manyetik olarak güçlendirilmiş kuadrupol kütle analizörleri ek bir manyetik alan içerirler, bu ek alan eksen veya en boyunca uygulanabilir. Yeni tip bu alet çözünürlük ve/veya hassaslık açısından ek bir perfromans sağladı. Çözünürlük ve hassaslık uygulanan manyetik alanın yön ve büyüklüğüne göre değişir.[19][20] Geçiş kuadrupolünün yaygın bir çeşidi olarak üçlü kuadrupol kütle spektrometreleri mevcuttur. "Üçlü kuad" birbirini izleyen üç adet kuadrupol basamağına sahiptir. Bu basamaklardan ilki ikinci kuadrupole gitmesi gereken belirli iyonların geçişini sağlar ve bu amaçla bir kütle filtresi gibi davranır. İkinci kuadrupole bir çarpışma çemberidir, çemberinde için iyonlar parçalara ayrılabilir. Üçüncü kuadrupol de bir kütle filtresi gibi işlev görür, belirli iyonların iyon detektörüne geçişini sağlar. Eğer bir kuadrupolüne bazı kütle filtresi ayarları aralığı ani ve tekrar ederek döngüler oluşturulursa, tüm spektra rapor edilebilir. Benzeri şekilde, bir üçlü kuad ile ardışık kütle spektrometrisi karakteri tipi taramalar yapılabilir.
Üç boyutlu kuadrupol iyon tuzağı
Paul tuzağı kuadrupol kütle analizörü ile aynı fiziksel presipleri paylaşır fakat iyonları yakalaması ve sonra düzenekten çıkartması özelliği yönünden farklı bir konuma sahiptir. İyonlar başlıca kuadrupol RF (Kuadrupol RF alanı,genellikle DC vya yardımcı AC potansiyellerine bağlı ,iki tane sonbaşlık elektrotunun arasındaki bir çember elektrotun içerisinde kalan alanı ifade eder) alanında tutulurlar. Numune dahili olarak (bir elektron veya lazer hüzmesi ile) veya harici olarak(bir sonbaşlık elektrotundaki bir açıklıktan alete giriş sağlanarak) iyonize edilir.
Birçok m/z ayırma ve izolasyon yöntemi mevcuttur. Ancak bunların en yaygın kullanılanı kütle kararsız modudur. Bu modda RF potansiyeli yükseltilir ve bundan dolayı a > b kütleli iyonların yörüngesi kararlı hale gelmişken, b kütleli iyonlar karasız hale gelmiş ve detektörün z-eksenine atılırlar. Aynı zamanda, yok edici olamayan analiz yöntemleri de vardır.
İyonlar rezonans heycanlanma metodu ile de atılabilir, bu durumda tamamlayıcı sonbaşlık elektrotlarına titreştiricisine heycanlanma voltajı uygulanır ve tuzaklama voltajı büyüklüğü ve/veya heycanlanma voltajı frekansı, m/z oranınca esasınca sıralanarak rezonans konumuna gelecek iyonlara göre değişir.[21][22]
Silindrik iyon tuzağı
Silindrik iyon tuzağı kütle spektrometresi (cylindrical ion trap mass spectrometer/CIT-MS) kuadrupol iyon tuzağının bir türevidir, farkı hiperbolik sekilli eltrotlardansa düz çemberlerden oluşan elektrotlar kullanıyor olmasıdır. Mimarisi minyatürleştirlmeye oldukça uygundur çünkü tuzağın boyutu düştükçe elektrik alanın şekli- iyonların yakalandığı- tuzak merkezine yaklaşır ve hiperbolik tuzağın şekline yakın bir şekil oluşur.
Lineer kuadrupol iyon tuzağı
Lineer kuadrupol iyon tuzağı kuadrupol iyon tuzağına benzer ancak 3D kuadrupol iyon tuzağında bulunan üç boyutlu kuadrupol alanı yerine iki boyutlu kuadrupol alan kullanarak iyonları tuzaklar. Thermo Fisher'ın LTQ ("Lineer tuzaklı kuadrupol-linear trap quadrupole") aleti lineer kuadrupol iyon tuzağına bir örnektir.[23]
Bir toroydal (halkasal) iyon tuzağı eğilmiş bir lineer kuadrupol şeklinde betimlenebilir. Bu tip iyon tuzağı, uçta toroyid şeklini oluşturarak dönen-donat şekilli- 3D iyon tuzağının sonuna bağlı olarak ya da enine kesitinde bulunur. Bu toroyidal şekilli tuzak kütle analizörünün ilerletilmiş seviyede minyatürleştirilmesine olanak sağlayan bir konfigürasyondur. Ek olarak, aynı tuzaklama alanında tutulan tüm iyonlar beraber atılırlar. Böylece oluşacak çeşitli dizilerin işlenmesi gibi karmaşık bir problem oluşmadan işlem basitçe gerçekleştirilmiş olur.[24]
Toroyidal tuzakta olduğu gibi, lineer tuzaklar ve 3D kuadrupol iyon tuzakları en çok minyatürize edilmiş kütle analizörleridir, sebep ise sahip oldukları yüksek hassalıkları, mTorr basıncına toleransları ve yalnız ardışık kütle spektrometrisindeki-ürün iyon taraması gibi- yetenekleridir.[25]
Orbitrap

Orbitrap aleti Fourier dönüşümü iyon siklotron rezonansı kütle spektrometresine (aşağıdakıdaki metine bkz.) benzerdir. İyonlar dingil şekilli bir elektrotu merkez alarak çevresinde elektrostatik olarak tuzaklanıp bir yörüngeye otururlar. Elektrot iyonları hapseder böylece ikisi birden(elektrot ve iyonlar) merkez elektrot çevresinde yörüngeye oturur. ve merkez elektrotun uzun olan eksenince bir ileri bir geri titreşirler. Titreşimler aletin üzerine kayıt yaptığı detektör tabağının üzerinde bir görüntü akımı oluşturur. Görüntü akımının frekansı iyonların m/z oranlarında bağlıdır. Kütle spektrumu kaydedilmiş görüntü akımının Fourier dönüşümü ile elde edilir.[26] Orbitrap yüksek kütle kesinliğine, yüksek hassaslığa ve iyi bir dinamik aralığına(menziline) sahiptir.
Fourier dönüşümü iyon siklotron rezonans
_Mass_spectrometer.jpg.webp)
Fourier dönüşümü iyon siklotron rezonans (Fourier transform mass spectrometry-FTMS),veya tam adıyla Fourier dönüşümü iyon siklotron rezonansı MS, kütleyi iyonların siklotronlaması ile üretilen görüntü akımını belirleyerek ölçer. Bir detektör (elektron multipleri) ile iyonların sapmalarını ölçmek yerine iyonlar bir Penning tuzağına (bir statik elektrik/manyetik iyon tuzağı) doldurulur. Penning tuzağında iyonlar etkin bir biçimde bir düzeneğin parçası haline gelir. Boşlukta sabitlenmiş pozisyondaki detektörler, kendilerine yakın noktalardan geçen iyonların elektrik sinyalini ölçer ve periyodik sinyaller üretir. İyonların döndürülmesinin frekansı m/z oranı tarafından belirlendiğinden, Fourier transfromu sinyaller üzerinde kullanılarak m/z oranı belirlenebilir. Fourier dönüşümü kütle spektrometrisi (Fourier transform mass spectrometry-FTMS) yüksek hassaslık (bir iyon birden fazla kere "hesap" edildiğinden), ve daha yüksek çözünürlüğe (daha ince ölçümler sağlar) sahip olmasından avantajlı konumdadır.[27][28]
İyon siklotron rezonansı (Ion cyclotron resonance-ICR) FTMS' e benzer ve daha eski bir tekniktir. FTMS' den farkı iyonları geleneksel bir detektör ile belirlemesidir. İyonlar Penning tuzağında bir RF elektrik alanı ile detektörün bulunduğu yer olan tuzak duvarına çarpıncaya kadar heycanlandırılır. Farklı kütlelere sahip iyonlar çarma zamalarına göre tespit edilir.
Dedektörler

Kütle spektrometrelerinin son parçası detektördür. Detektör tetiklenmiş yükleri veya bir iyon geçişi ile veya yüzeye çarpması ile üretilmiş olan akımı ölçer. Bir tarama aletinde, tarama boyunca detektörde üretilen sinyale karşı enstrumanın tarama yaptığı nokta(taramadaki m/Q noktası) bir kütle spektrumu üretir. Bu spektrum, iyonların m/Q' nun bir fonksiyonu şeklindeki kaydıdır.
Tipik olarak, elektron multiplerleri detektör olarak kullanılmasına karşın, Faraday kupası ve iyon-foton detektörlerinin de kullanımı mevcuttur. Genelde kütle analizöründen ayrılan iyon sayısı çok azdır ve bundan dolayı sinyal eldesi için kaile alınır bir arttırma(sinyal) işlemine ihtiyaç duyulur. Mikrokanal plaka dedektörleri modern cihazların içerisinde sıkça kullanılır.[29] Fourier dönüşümü kütle spektrometrisi ve orbitraplarda, dedektörler parçacıkların titreyerek yakınından geçtiği kütle analizörü/iyon tuzağı alanının içinde bulunan bir çift Faraday metal yüzeyinden oluşur. Direkt akım oluşmaz, sadece zayıf bir alternatif akım elektrotlar arasındaki bir düzenekte üretilir. Diğer uyarımsal detektörler de kullanımdadır.[30]
Ardışık kütle spektrometrisi

Ardışık kütle spektrometrisi birden çok sefer kütle spektrometrisi sağlayan araçtır. Genellikle bu farklı spektrometriler bazı molekül parçalarının oluşumu ile birbirinden ayrılır. Örneğin, bir kütle analizörü alete giren diğer bileşenlerden bir peptidi izole ederken ikinci kütle analizörü peptit iyonları gala çarpışırken peptit iyonlarını stabilize ederek bu iyonların çarpışmaya bağlı ayrışmasına (Collision-Induced Dissociation-CID) sebebiyet verir. Üçüncü kütle analizörü peptitten çıkan parçaları işler (sıralar). Ardışık MS aynı zamanda aynı kütle analizörünün tekrarı ile de oluşturulabilir, Paul tuzağında olduğu gibi. Çarpışmaya bağlı ayrışma, elektron yakalama ayrışması (Electron Capture Dissociation-ECD), elektron transfer ayrışması (Electron Transfer Dissociation-ETD), kızılötesi multifoton ayrışma (Infrared Multiphoton Dissociation-IRMPD), kara cisim kızılötesi ışınım ayrışması (Blackbody Infrared Radiative Dissociation-BIRD), elektron koparma ayrışması (Electron-Detachment Dissociation-EDD) ve yüzey kaynaklı ayrışma (Surface-Induced Dissociation-SID) gibi teknikler ardışık MS için var olan molekül parçalama yöntemleridir. Ardışık MS' i kullanan önemli uygulamalardan biri protein karekterizasyonudur.[31]
Ardışık MS çeşitli deney dizilerini imkânlı kılar. Çoğu ticari MS rutin dizileri (seçilmiş reaksiyon izleme (Selected Reaction Monitoring-SRM) ve ata iyon tarama gibi) işlemeyi hızlandırmak için tasarlanmıştır. SRM' de ilk analizör sadece bir kütlesinin kendi içinden geçişine müsaade eder. İkinci analizör ise kullanıcının seçtiği birçok parça iyondan sorumludur. İkinci kütle anlizinin görev döngüsü kısıtlı olduğunda SRM genellikle bir tarama cihazı ile beraber kullanılır. Bu deneyler bilinen molküllerin belirlenmesinde spesifikliği arttırmak amaçlı kullanılır, özellikle farmakokinetik çalışmalarda bu durum ön plandadır. Ata iyon tarama ata iyondan spesifik bir kaybın aranışı için yapılan görütülenmesidir. İlk ve ikinci kütle analizörleri kullanıcı tarafından belirlenmiş m/z değerini kapsayan spektrum boyunca tarama yaparlar. Bu deney bilinmeyen moleküllerde spesifik bir motif tanımlama amacı ile kullanılır.
Hızlandırıcı MS (accelerator mass spectrometry-AMS) radyokarbon tarihleme için kullanılır. Bu ardışık MS türü negatif iyonları bir ardışık MS' e doğru hızlandırmak için genelde mega-volt seviyelerinde çok yüksek voltajlar kullanılır.
Yaygın kütle spektrometre konfigürasyonları ve teknikleri
Bir kaynak, analizör ve detektör komibasyonu yaygın olarak kullanılmaya başlandığında bu kombinasyona bileşenlerin isimlerinin kısaltmalarından yeni bir kısa isim türetilir. Buna örenek olarak MALDI-TOF mevcuttur. Bu ikili isim MALDI iyonizasyon kaynağı ve TOF kütle analizörünün kombinasyonunu ifade eder. Diğer örnekler arasında tetikli bir şekilde eşlenmiş plasma-kütle spektrometrisi (coupled plasma-mass spectrometry (ICP-MS)), AMS, Termal iyonizasyon-MS (thermal ionization-mass spectrometry (TIMS)) ve kıvılcım kaynağı-MS (spark source mass spectrometry (SSMS)) bulunur.
MS ile kombine edilmiş ayırma teknikleri
MS' i kütle belirleme ve kütle çözünürlüğünde güçlendirmek için MS' e ardışık kromatografik ve diğer ayrım tekniklerinin kullanılır.
Gaz kromatografisi

Yukarıda bahis geçen yaygın kombinasyonlardan biri gaz kromatografisi-kütle spektrometrisi (GC/MS ve GC-MS). Bu teknikte gaz kromatografisi farklı bileşikleri ayırmak amacı ile kullanılır. Ayrılmış bileşiklerin buharı iyon kaynağına(voltaj uygulanan bir metal filament) yönlendirilir. Bu filament bileşiklerin iyonlaşmasını sağlayan elektronları yayar. İyonlar yine iyonlaşarak parçalar oluşturabilir ve tahmin edilebilir modeller oluştururlar. Bütün haldeki iyon ve parçalar önce MS' in analizörüne ve en sonunda teşhis edilirler.[32]
Sıvı kromatografisi

GC-MS' e benzer olarak sıvı kromatografisi-kütle spektrometrisi (liquid chromatography-mass spectrometry (LC/MS veya LC-MS)) bileşikleri kromatografik olarak ayırır, bu işlem bileşikler iyon kaynağı ve kütle analizörüne girmeden gerçekleşir. GC-MS' den mobil fazının sıvı olması ile farklıdır. Bu sıvı faz genelde su ve -gaz yerine- bir organik çözücünün karışımıdır. En yaygın LC-MS, sıvı kromatografisi ile ESI' nin kombinasyonudur. Diğer kombinasyonlar ise APCI ve APP iyonizasyon kaynaklarını içerir. Bunların yanı sıra yeni geliştirilmiş teknikler de sıvı kromatografisi ile kombine edilir, lazer sprey gibi.
Kapiler elektroforez–kütle spektrometrisi
Kapiler elektroforez–kütle spektrometrisi (Capillary electrophoresis–mass spectrometry (CE-MS)) kapiler elektroforezin sıvı ayırma işlemini MS ile kombine eden bir tekniktir.[33] CE-MS genellikle ESI ile kombine edilir.[34]
İyon hareketliliği
İyon hareketlilik spektrometrisi-kütle spektrometrisi (Ion mobility spectrometry-mass spectrometry (IMS/MS veya IMMS)), iyonları MS' e girmeden bir nötral gaz içinde ve bir uygulanmış elektriksel potansiyel gradiantı varlığında birbirinden ayıran bir tekniktir.[35] Sürükllenme süresi iyonun yarıçap/yük oranı ile ilişkilidir. IMS' in görev döngüsü (deneyin gerçekleştiği süre) çoğu MS tekniğinden uzundur. Normal bir MS işini IMS ayırma işlemini tamamlayana değinki sürede bitirir. Teknik, LC-MS' benzer şekilde, IMS ayırması ve m/z oranı hakkında veri üretimi sağlar.[36]
IMS'nin görev döngüsü, sıvı kromatografisine veya gaz kromatografisi ayırmalarına göre kısadır ve bu nedenle bu iki tekniğe bağlanarak LC/IMS/M gibi üçlü yöntemler üretebilir.[37]
Veri ve analiz

Veri sunumları
Kütle spektrometrisi çeşitli veriler üretir. En yaygın veri sunum şekli kütle spektrumudur.
Belli MS veri tipleri en iyi şekilde bir kütle kromatogramı şeklinde sunulur. Bu kromatogramlar arasında seçilmiş iyon izleme (selected ion monitoring-SIM), total iyon akımı (total ion current-TIC) ve seçilmiş reaksiyon izleme (selected reaction monitoring-SRM) yer alır.
Diğer MS veri tipleri 3D kontur haritaları şeklinde iyi bir şekilde ifade edilir. Bu durumda, m/z oranı x-eksenine, yoğunluk y-eksenine ve zaman gibi ek bir parametre z- ekseni üzerine kaydedilir.
Veri analizi
MS veri analizi veriyi üreten deneye özgüdür. Verinin genel altbölünmesi her veriyi analamak üzerine temellenmiştir.
Çoğu MS hem negatif iyon modu veya pozitif iyon modunda çalışabilme yeteneğine sahiptir. Bu yetenek gözlenen iyonların pozitif mi yoksa negatif mi olduğunu anlamak açısından çok önemlidir. Genellikle bu durum nötral kütleyi hesaplamakta çok önemli olsa da aynı zamanda molekülün doğası hakkında ipuçları da verir.
Farklı tip iyon kaynakları-orijinal molekülden üretilmiş- birbirinden farklı bir dizi parçacık oluşumu ile sonuçlanır. Bir elektron iyonlaştırma kaynağı birçok parça (çoğu tek yüklü (-1) radikaller) üretirken ESI genellikle radikal olmayan yarımoleküler iyonlar üretir, bu moleküller genelde multi yüklüdür. Ardışık MS amaç olarak parça iyonları kaynak-sonrası üretir ve deney tarafından üretilen verinin çeşidini şiddetli bir şekilde değiştirebilir.
Numunenin kökeni hakkında bilgi molekülün bileşenleri ve parçaları hakkında bilgi sağlayabilir. Bir sentez/imalat işlemi ürünü numunesi hedef molekül çevresinde düşünüldüğünde kimyasal safsızlıklar içerecektir. Ham bir şekilde hazırlanmış biyolojik numuneler muhtemelen belli bir miktarda tuz içerecektir. Bu tuz, belli analizlerde, analit molekülle birleşerek bir birleşim ürünü oluşturabilir.
Sonuçlar aynı zamanda numunenin nasıl hazırlandığına ve ne şekilde MS' e sokulduğu ile de ilşkilidir. Bunun önemli bir örneği, MALDI noktalaması için kullanılan matrikstir, matriks yayılım/iyonlaşma olayı enerjisinin kontrolünde lazerden daha önemlii bir faktördür. Bazen numuler sodyum veya diğer iyon taşıyan türlerle muamele edilir ve böylece, protone edilmiş türler yerine, toplanma ürünleri elde edilmiş olur.
MS molar kütleyi ve numune saflığını ölçebilir ve moleküler yapıyı çözebilir. Her bir ölçüm hedefi farklı bir deneysel prosedürü yanında getirir. Bundan dolayı deney amacının uygun şekilde tanımlanması doğru veri toplamak ve verileri doğru şekilde yorumlamak için bir önkoşuldur.
Kütle spektrumunun yorumlanması
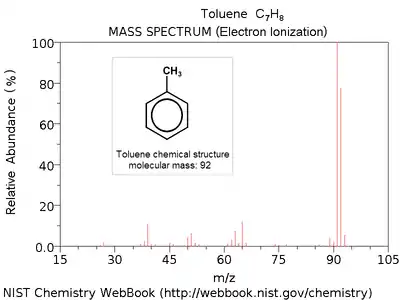
Moleküllerin kesin yapıları ve peptid dizileri parça kütleleri setleri ile deşifre edildiğinden, kütle spektrumunun yorumu çeşitli tekniklerin kombinasyonunu gerektirir. Genellikle bilinmeyen bir bileşiğin kütlesini belirlemek için ilk strateji bileşiğin deneysel kütle spektrumunu kütle spektrum kütüphanesi ile karşılaştırmaktır. Eğer eşleşme yoksa, ya manuel yorumlamaya geçilir[38] ya da yazılım yardımlı ile kütle spektrasının yorumlanması yapılır. MS' te olan iyonizasyon ve parçalanmanın bilgisayar simülasyonu peptid yapısı veya dizisinden bir moleküle kadar tanımlama yapmak için kullanılacak ilk araçtır. Bir önsel yapısal bilgi in silico (bilgisayarda) parçalanır ve sonuç gözlenen spektrum ile karşılaştırılır. Böyle similasyonlar genelde bir parçalama kütüphanesi tarafından desteklenir.[39] Kütüphane bilinen parçalanma reaksiyonlarını içerir. Hem ufak moleküller hem de proteinler için geliştirilmiş bu fikir MS yazılımını avatajlı kılar.
Kütle spektra analizi kesin kütle spektrası ile de olabilir. Sadece bir tam sayı m/z oranı ile iyon yapısının teoritik olarak mümkün bir mükemmel sayı ile ifade edilebilir. Ancak, daha hassas kütle figürleri aday moleküler formülün sayısını azaltır. Formül oluşturucu adındaki bilgisayar algoritması verilen kütle ile ona özel tanımlanmış toleransa uygun şekülde teorik olarak bütün moleküler formülleri hesaplar.
Ata iyon parmak izi MS' te yapı çıkarımı yapmak için yeni çıkarılmış bir tekniktir. Teknik yapısal bilginin bireysel parçalarını belirler ve onları molekülün ardışık spektra araması ile bağdaştırır. Bu aramada yapısal olarak karakterize edilmiş ata iyonların ürün iyon spektrası kütüphanesi ile karşılaştırma yapılır.[40]
Uygulamalar

Kütle spektrometrisi hem nitel hem nicel amaçlı kullanıma sahiptir. Bu kullanımlara bilinmeyen bir bileşiğin tanımlanması, bir molekülün içerisindeki elementlerin izotopik içeriklerinin belirlenmesi ve bir bileşiğin parçalanmasının gözlenmesiyle yapısının tanımlanması dahildir. Diğer kullanımlar arasında bir numune içerisindeki bir bileşiğin miktarının belirlenmesi veya gaz fazı iyon kimyası (bir vakum içindeki nötral ve iyonların kimyası) temelleri çalışmaları bulunur. MS şu anda, birçok çeşit bileşiğin fiziksel, kimyasal veya biyojik özellikleri üzerine çalışmalar yapan analitik laboratuvarlarda yaygın bir biçimde kullanılır.
Bir analitik teknik olarak MS, diğer benzeri tekniklerden farklı avatajlara sahiptir. Bu avantajlardan arasında MS' in bir analiz cihazının, bir kütle-yük filtresi gibi, arka plan müdehalelerini azaltmasından dolayı birçok diğer analitik teknikten daha yüksek hassaslığa sahip olması, bilinmeyen bir bileşiğin tanımlanması ya da şüphelenilen bileşiklerin numunedeki varlığının onaylanması için karakteristik parçalanmalar üretmesinden doğan mükemmel özgüllüğü, moleküllerin moleküler ağırlığı ve elementlerin izotopik bollukları hakında bilgi verebilmesinin yanı sıra geçici çözümlenmiş kimyasal veriler sağlaması vardır.
Bu metodun birkaç dezaavantajı arasında optik ve geometrik izomerleri birbirinden ayırmakta ve aromatik halkadaki o-, m- ve p- dallanma pozisyonlarını birbirinden ayırmakta başarısız olması bulunur. Buna ek olarak, metot benzer parçalanmış iyonlar üreten hidrokarbonları tanımlamada kısıtlı bir kapsama sahiptir.
İzotop oranı MS: izotop tarihleme ve izsürme

MS aynı zamanda numune içindeki elementlerin izotopik içeriklerinin belirlenmesi için de kullanılır. Bir elementin izotopları arasındaki kütle farkı oldukça azdır ve bir elementin daha az yaygın bulunan izotopları çok nadirlerdir ve bundan dolayı çok hassas bir alete ihtiyaç vardır. Bu aletler, bazen İzotop oranı kütle spektrometresi (isotope ratio mass spectrometers, kısaca IR-MS) şeklinde hitap edilirler. Bu tip MS genellikle, iyonize parçacıkları, parçacık darbelerini elektrik akımına dönüştüren, bir dizi Faraday kupasına doğru yönlendirmek için bir magnet bulundurur. Suyun deuterium içerik analizi hızlı bir şekilde bilgisayar kontrolünde akıcı görüntü tutulması kütle spektrometrisi (flowing afterglow mass spectrometry, FA-MS) kullanılarak başarılabilir. Muhtemelen bu amaca uygun en hassas ve kesin kütle spektrometresi hızlandırıcı kütle spektrometresidir (accelerator mass spectrometer, AMS). Bunun sebebi AMS' nin en yüksek hassaslığı sağlaması, atomları birey atomlar halinde ölçebiliyor olması ve ana kararlı izotopa göre 1015 civarı dinamik menzilli nüklidleri ölçebilmesidir.[41] İzotop oranları çeşitli işlemlerin önemli işaretçileridir. Bazı izotop oranları, karbon tarihlemedeki gibi, nesnenin yaşını belirlemede kullanılır. Buna ilave olarak, kararlı izotoplar ile etiketleme ise protein miktar belirlenmesi amacı ile kullanılır (aşağıdaki, protein karakterizasyonu bölümüne bakınız).
Membran girişli kütle spektrometrisi: Çözeltideki gazları ölçme
Membran girişli kütle spektrometrisi, izotop oranı MS ile bir gaz geçirgen membran tarafından ayrılmış bir tepkime bölme/hücresini birleştirir. Bu yöntem çözeltilerin içinde gelişen gazların üzerinde çalışılmasına olanak sağlar. Yöntem, Fotosistem II' nin oksijen üretiminin üzerinde yapılan çalışmalarda yaygın bir şekilde kullanılmıştır.[42]
İzmiktar gaz analizi
Bir akış veya kayış tüpüne aktarılmış bir iyon kaynağında üretilen iyonları kullanan birkaç teknik vardır, seçilmiş iyon akış tüpünü kullanan seçilmiş iyon akış tüpü MS (selected ion flow tube, SIFT-MS) ve proton transfer tepkimesinden faydalanan proton transfer tepkimesi MS (proton transfer reaction, PTR-MS). Bu teknikler hava, nefes veya sıvı kafaboşluğunun izmiktar gaz analizi için kullanılan kimyasal iyonizasyonun çeşitleridir. Çok hassas bir şekilde belirlenmiş bir tepkime süresi kullandıklarından bilinen bir reaksiyon kinetiğinin kullanımı ile iç standart veya kalibrasyon olmaksızın analit konsantrasyonu hesaplanabilir.
Atom probu
Atom probu, Birey atomların konumlarını haritalandırmak amacı ile TOF-MS ile alan buharlaştırma mikroskopisini birleştirmiş alettir.
Farmakokinetik
Farmakokinetik matriksin (kan ve idrar) kompleks yapısından dolayı, düşük doz/uzun zaman noktası verilerin, gözlemlemek amaçlı yüksek hassaslık ihtiyacı için sıkça MS ile çalışılır. Bu amaçla en yaygın kullanılan alet üçlü kuadrupol MS' li LC-MS' tir. Ardışık MS genelde özgüllük katma amacı ile kullanılır. Standart eğrileri ve iç standartlardan numunedeki tek bir farmasötiğin miktarının belirlenmesinde faydalanılır. Birer farmasötik olarak farklı zaman noktalarını temsil eden numuneler uygulanıp ardından metabolize edilir veya vücuttan temizlenirler. curves and internal standards are used for quantitation of usually a single pharmaceutical in the samples. The samples represent different time points as a pharmaceutical is administered and then metabolized or cleared from the body. Uygulamadan önce alınan blank (kelime anlamı boş) veya diğer bir tabirle t=0 numuneleri karışık matriksli numunelerde arka planı belirlemekte ve veri bütünlüğünden emin olmakta önem ifade eder. Standart eğrinin lineerliğine çok dikkat edilir ancak daha karışık fonksiyonlu, kuadritikler gibi, eğri uydurma kullanımı yaygın değildir. Bunun sebebi çoğu MS' in yanıtı yüksek konsantrasyon aralıklarında lineerden daha düşüktür.[43][44][45]
Güncel olarak, hayvan deneylerine bir alternatif olarak görülen, mikrodozlama çalışmaları için aşırı hassas MS kullanımına kaile alınır derecede ilgi mevcuttur.
Protein karakterizasyonu
MS proteinlerin dizilenmesi ve karakterize edilmeleri için önemli bir tekniktir. Bütün proteinlerin iyonizasyonu için iki ana yöntem vardır, ESI ve MALDI. Performans ve MS' ler için mümkün olan kütle aralığı göz önüne alındığında protein karaktrizasyonu için iki yaklaşım vardır. İlki, yekpare proteinlerin MALDI veya ESI ile iyonlaştırılması ve ardından kütle analizörüne girmeleridir. Bu yaklaşım üst-alt stratejisi olarak bilinir. Üst-alt yaklaşımı çoğu zaman az verili tek protein çalışmaları ile sınırlıdır. İkincisi yaklaşımda ise proteinler elektroforetik ayrımdan sonra bir jelde veya çözeltide enzimatik olarak sindirilip küçük peptitlere dönüştürülürler. Sonrasında peptitlerin hepsi kütle analizörüne yönlendirilir. Eğer protein kimiklendirmesi için karakteristik bir peptit şablonu kullanılıyorsa yöntem peptid kütle parmak izi (Peptide Mass Fingerprinting, PMF) adını alır. Eğer ki kimliklendirme ardışık MS analizinde belirlenmiş dizi verisini kullanıyorsa yöntem de novo peptid dizileme olarak adlandırılır. Bu protein analizi prosedürleri aynı zamanda "alt-üst" yaklaşımı olarak anılır. Daha yeni kullanılmaya başlanan üçüncü bir yaklaşım ise "orta-alt" yaklaşımıdır. Bu yaklaşım tipik triptik peptitlerden daha büyük proteolitik peptitlerin incelenmesini içerir.[46]
Glikan analizi
Düşük numune ihtiyacı ve yüksek hassalığı sebebi ile MS glikobiyolojide glikan yapıların açıklanması ve karakterizasyonu için sıkça kullanılır.[47] MS glikanların analizi için HPLC' yi tamamlayıcı metot olarak kullanılır. Tüm haldeki glikanlar MALDI-MS ile tek yüklü iyon olarak belirlenebilirler veya permetilasyon ve perasetilasyonu takiben, hızlı atom bombardımanı MS (fast atom bombardment mass spectrometry, FAB-MS) aracılığıyla belirlenebilirler.[48] Bunlara ek olarak ise ESI-MS küçük glikanlar için güçlü sinyaller verir.[49] Glikan yapı karakterizasyonuna yardımcı ve MS verisini yorumlayan çeşitli bedava ve ticari yazılımlar mevcuttur.
Uzay Keşifleri

Analiz için standart bir yöntem olarak MS, diğer gezegen ve uydulara ulaştı. 2 tanesi Viking programı ile Mars' a gönderildi. 2005' in başlarında Cassini–Huygens görevi kapsamında özelleştirilmiş bir GC-MS aleti, Satürn' ün en büyük uydusu, Titan' ın atomosferinden Huygens probuna teslim edildi. Bu alet iniş rotası boyunca atmosferik numuneleri analiz etti. Prob indiğinde alet Titan' ın donmuş hidrokarbon kaplı yüzeyini buharlaştırıp analiz edebiliyordu. Bu ölçümler her parçacığın izotopik oranlarını Dünya' daki doğal izotopik oranla karşılaştırıyordu.[50] Cassini–Huygens uzay aracındaki MS, bir iyon ve nötral MS olmasının yanında aynı zamanda Enceladus bulutlarının içeriğinide inceliyordu. Mars Phoenix uzay aracı, 2007' de çalıştırılmaya başlanmış, bir Termal ve Gelişmiş Gaz Analizör MS taşıyordu.[51]
Aynı zamanda MS uzay görevlerinde plazmaların içeriklerini ölçmek içinde kullanılır. Örneğin, Cassini uzay aracının taşıdığı Cassini Plazma Spectrometresi (Cassini Plasma Spectrometer, CAPS),[52] Satürn' ün manyetosferindeki iyonların ağırlığını ölçüyordu.
Ayrıca bakınız
Kaynakça
- Sparkman, O. David (2000). Mass spectrometry desk reference. Pittsburgh: Global View Pub. ISBN 0-9660813-2-3.
- "Definition of spectrograph". Merriam Webster. 1 Şubat 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 1 Şubat 2020.
- Downard, Kevin (2004). "Mass Spectrometry - A Foundation Course". Royal Society of Chemistry. doi:10.1039/9781847551306. ISBN 978-0-85404-609-6.
- Squires, Gordon (1998). "Francis Aston and the mass spectrograph". Dalton Transactions, 23. ss. 3893-3900. doi:10.1039/a804629h.
- Downard KM (2007). "Historical account: Francis William Aston: the man behind the mass spectrograph". European Journal of Mass Spectrometry. 13 (3). ss. 177-90. doi:10.1255/ejms.878. PMID 17881785.
- Thomson, J.J. (1913). Rays Of Positive Electricity and Their Application to Chemical Analysis. Londra: Longman's Green and Company.
- Siri, William (1947). "Mass spectroscope for analysis in the low-mass range". Review of Scientific Instruments. 18 (8). ss. 540-545. Bibcode:1947RScI...18..540S. doi:10.1063/1.1740998.
- Price P (Ağustos 1991). "Standard definitions of terms relating to mass spectrometry : A report from the committee on measurements and standards of the American society for mass spectrometry". Journal of the American Society for Mass Spectrometry. 2 (4). ss. 336-48. doi:10.1016/1044-0305(91)80025-3. PMID 24242353.
- Parkins, William E. (2005). "The uranium bomb, the calutron, and the space-charge problem". Physics Today. 58 (5). ss. 45-51. Bibcode:2005PhT....58e..45P. CiteSeerX 10.1.1.579.4119 $2. doi:10.1063/1.1995747. ISSN 0031-9228.
- "The Nobel Prize in Chemistry 2002: Information for the Public". The Nobel Foundation. 9 Ekim 2002. Erişim tarihi: 29 Ağustos 2007.
- Fenn JB, Mann M, Meng CK, Wong SF, Whitehouse CM (Ekim 1989). "Electrospray ionization for mass spectrometry of large biomolecules". Science. 246 (4926). ss. 64-71. Bibcode:1989Sci...246...64F. doi:10.1126/science.2675315. PMID 2675315.
- Tanaka K, Waki H, Ido Y, Akita S, Yoshida Y, Yoshida T (1988). "Protein and Polymer Analyses up to m/z 100 000 by Laser Ionization Time-of flight Mass Spectrometry". Rapid Commun Mass Spectrom. 2 (20). ss. 151-3. Bibcode:1988RCMS....2..151T. doi:10.1002/rcm.1290020802.
- Karas M, Bachman D, Bahr U, Hillenkamp F (1987). "Matrix-Assisted Ultraviolet Laser Desorption of Non-Volatile Compounds". Int J Mass Spectrom Ion Proc. Cilt 78. ss. 53-68. Bibcode:1987IJMSI..78...53K. doi:10.1016/0168-1176(87)87041-6.
- Osborn DL, Zou P, Johnsen H, Hayden CC, Taatjes CA, Knyazev VD, North SW, Peterka DS, Ahmed M, Leone SR (Ekim 2008). "The multiplexed chemical kinetic photoionization mass spectrometer: a new approach to isomer-resolved chemical kinetics". Review of Scientific Instruments. 79 (10). s. 104103. Bibcode:2008RScI...79j4103O. doi:10.1063/1.3000004. PMID 19044733.
- Bruins, A. P. (1991). "Mass spectrometry with ion sources operating at atmospheric pressure". Mass Spectrometry Reviews. 10 (1). ss. 53-77. Bibcode:1991MSRv...10...53B. doi:10.1002/mas.1280100104.
- Cottrell JS, Greathead RJ (1986). "Extending the Mass Range of a Sector Mass Spectrometer". Mass Spectrometry Reviews. 5 (3). ss. 215-247. Bibcode:1986MSRv....5..215C. doi:10.1002/mas.1280050302.
- In the event that the ions do not start at identical kinetic energies, some ions may lag behind higher kinetic energy ions decreasing resolution. Reflectron geometries are commonly employed to correct this problem. Wollnik, H. (1993). "Time-of-flight mass analyzers". Mass Spectrometry Reviews. 12 (2). ss. 89-114. Bibcode:1993MSRv...12...89W. doi:10.1002/mas.1280120202.
- Guilhaus, Michae. "Principles and Instrumentation in Time-of-flight Mass Spectrometry" (PDF). JOURNAL OF MASS SPECTROMETRY. Cilt 30. ss. 1519È1532 – Google Scholar vasıtasıyla.
- Syed SU, Maher S, Taylor S (Aralık 2013). "Quadrupole mass filter operation under the influence of magnetic field". Journal of Mass Spectrometry. 48 (12). ss. 1325-39. Bibcode:2013JMSp...48.1325S. doi:10.1002/jms.3293. PMID 24338888.
- Maher S, Syed SU, Hughes DM, Gibson JR, Taylor S (Ağustos 2013). "Mapping the stability diagram of a quadrupole mass spectrometer with a static transverse magnetic field applied". Journal of the American Society for Mass Spectrometry. 24 (8). ss. 1307-14. Bibcode:2013JASMS..24.1307M. doi:10.1007/s13361-013-0654-5. PMID 23720050.
- Paul W, Steinwedel H (1953). "Ein neues Massenspektrometer ohne Magnetfeld". Zeitschrift für Naturforschung A. 8 (7). ss. 448-450. Bibcode:1953ZNatA...8..448P. doi:10.1515/zna-1953-0710.
- March RE (2000). "Quadrupole ion trap mass spectrometry: a view at the turn of the century". International Journal of Mass Spectrometry. 200 (1–3). ss. 285-312. Bibcode:2000IJMSp.200..285M. doi:10.1016/S1387-3806(00)00345-6.
- Schwartz JC, Senko MW, Syka JE (Haziran 2002). "A two-dimensional quadrupole ion trap mass spectrometer". Journal of the American Society for Mass Spectrometry. 13 (6). ss. 659-69. doi:10.1016/S1044-0305(02)00384-7. PMID 12056566.
- Lammert SA, Rockwood AA, Wang M, Lee ML, Lee ED, Tolley SE, Oliphant JR, Jones JL, Waite RW (Temmuz 2006). "Miniature toroidal radio frequency ion trap mass analyzer". Journal of the American Society for Mass Spectrometry. 17 (7). ss. 916-922. doi:10.1016/j.jasms.2006.02.009. PMID 16697659.
- Snyder DT, Pulliam CJ, Ouyang Z, Cooks RG (Ocak 2016). "Miniature and Fieldable Mass Spectrometers: Recent Advances". Analytical Chemistry. 88 (1). ss. 2-29. doi:10.1021/acs.analchem.5b03070. PMC 5364034 $2. PMID 26422665.
- Hu Q, Noll RJ, Li H, Makarov A, Hardman M, Graham Cooks R (Nisan 2005). "The Orbitrap: a new mass spectrometer". Journal of Mass Spectrometry. 40 (4). ss. 430-43. Bibcode:2005JMSp...40..430H. doi:10.1002/jms.856. PMID 15838939.
- Comisarow MB, Marshall AG (1974). "Fourier transform ion cyclotron resonance spectroscopy". Chemical Physics Letters. 25 (2). ss. 282-283. Bibcode:1974CPL....25..282C. doi:10.1016/0009-2614(74)89137-2.
- Marshall AG, Hendrickson CL, Jackson GS (1998). "Fourier transform ion cyclotron resonance mass spectrometry: a primer". Mass Spectrometry Reviews. 17 (1). ss. 1-35. Bibcode:1998MSRv...17....1M. doi:10.1002/(SICI)1098-2787(1998)17:1<1::AID-MAS1>3.0.CO;2-K. PMID 9768511.
- Dubois F, Knochenmuss R, Zenobi R, Brunelle A, Deprun C, Le Beyec Y (1999). "A comparison between ion-to-photon and microchannel plate detectors". Rapid Communications in Mass Spectrometry. 13 (9). ss. 786-791. doi:10.1002/(SICI)1097-0231(19990515)13:9<786::AID-RCM566>3.0.CO;2-3.
- Park MA, Callahan JH, Vertes A (1994). "An inductive detector for time-of-flight mass spectrometry". Rapid Communications in Mass Spectrometry. 8 (4). ss. 317-322. Bibcode:1994RCMS....8..317P. doi:10.1002/rcm.1290080407.
- Boyd, Robert K. (1994). "Linked-scan techniques for MS/MS using tandem-in-space instruments". Mass Spectrometry Reviews. 13 (5–6). ss. 359-410. Bibcode:1994MSRv...13..359B. doi:10.1002/mas.1280130502.
- Eiceman, G.A. (2000). Gas Chromatography. In R.A. Meyers (Ed.), Encyclopedia of Analytical Chemistry: Applications, Theory, and Instrumentation, pp. 10627. Chichester: Wiley. 0-471-97670-9
- Loo JA, Udseth HR, Smith RD (Haziran 1989). "Peptide and protein analysis by electrospray ionization-mass spectrometry and capillary electrophoresis-mass spectrometry". Analytical Biochemistry. 179 (2). ss. 404-12. doi:10.1016/0003-2697(89)90153-X. PMID 2774189.
- Maxwell EJ, Chen DD (Ekim 2008). "Twenty years of interface development for capillary electrophoresis-electrospray ionization-mass spectrometry". Analytica Chimica Acta. 627 (1). ss. 25-33. doi:10.1016/j.aca.2008.06.034. PMID 18790125.
- Verbeck GF, Ruotolo BT, Sawyer HA, Gillig KJ, Russell DH (Haziran 2002). "A fundamental introduction to ion mobility mass spectrometry applied to the analysis of biomolecules". Journal of Biomolecular Techniques. 13 (2). ss. 56-61. PMC 2279851 $2. PMID 19498967.
- Matz LM, Asbury GR, Hill HH (2002). "Two-dimensional separations with electrospray ionization ambient pressure high-resolution ion mobility spectrometry/quadrupole mass spectrometry". Rapid Communications in Mass Spectrometry. 16 (7). ss. 670-5. Bibcode:2002RCMS...16..670M. doi:10.1002/rcm.623. PMID 11921245.
- Sowell RA, Koeniger SL, Valentine SJ, Moon MH, Clemmer DE (Eylül 2004). "Nanoflow LC/IMS-MS and LC/IMS-CID/MS of protein mixtures". Journal of the American Society for Mass Spectrometry. 15 (9). ss. 1341-53. doi:10.1016/j.jasms.2004.06.014. PMID 15337515.
- Tureček F, McLafferty FW (1993). Interpretation of mass spectra. Sausalito: University Science Books. ISBN 0-935702-25-3.
- Mistrik, Robert (2004). "A New Concept for the Interpretation of Mass Spectra Based on a Combination of a Fragmentation Mechanism Database and a Computer Expert System". Ashcroft, Alison E.; Brenton, G.; Monaghan, J.J. (Edl.). Advances in Mass Spectrometry. 16. Elsevier. s. 821. 11 Ocak 2012 tarihinde kaynağından arşivlendi.
- Sheldon MT, Mistrik R, Croley TR (Mart 2009). "Determination of ion structures in structurally related compounds using precursor ion fingerprinting". Journal of the American Society for Mass Spectrometry. 20 (3). ss. 370-6. doi:10.1016/j.jasms.2008.10.017. PMID 19041260.
- Maher S, Jjunju FP, Taylor S (2015). "100 years of mass spectrometry: Perspectives and future trends". Rev. Mod. Phys. 87 (1). ss. 113-135. Bibcode:2015RvMP...87..113M. doi:10.1103/RevModPhys.87.113.
- Shevela D, Messinger J (Kasım 2013). "Studying the oxidation of water to molecular oxygen in photosynthetic and artificial systems by time-resolved membrane-inlet mass spectrometry". Frontiers in Plant Science (İngilizce). Cilt 4. s. 473. doi:10.3389/fpls.2013.00473. PMC 3840314 $2. PMID 24324477.
- Hsieh Y, Korfmacher WA (Haziran 2006). "Increasing speed and throughput when using HPLC-MS/MS systems for drug metabolism and pharmacokinetic screening". Current Drug Metabolism. 7 (5). ss. 479-89. doi:10.2174/138920006777697963. PMID 16787157.
- Covey TR, Lee ED, Henion JD (Ekim 1986). "High-speed liquid chromatography/tandem mass spectrometry for the determination of drugs in biological samples". Analytical Chemistry. 58 (12). ss. 2453-60. doi:10.1021/ac00125a022. PMID 3789400.
- Covey TR, Crowther JB, Dewey EA, Henion JD (Şubat 1985). "Thermospray liquid chromatography/mass spectrometry determination of drugs and their metabolites in biological fluids". Analytical Chemistry. 57 (2). ss. 474-81. doi:10.1021/ac50001a036. PMID 3977076.
- Chait BT (2011). "Mass spectrometry in the postgenomic era". Annual Review of Biochemistry. Cilt 80. ss. 239-46. doi:10.1146/annurev-biochem-110810-095744. PMID 21675917. – via Annual Reviews (abonelik gereklidir)
- Apte A, Meitei NS (2009). Bioinformatics in glycomics: glycan characterization with mass spectrometric data using SimGlycan. Methods in Molecular Biology. 600. ss. 269-81. doi:10.1007/978-1-60761-454-8_19. ISBN 978-1-60761-453-1. PMID 19882135.
- Harvey DJ, Dwek RA, Rudd PM (Mart 2006). Determining the structure of glycan moieties by mass spectrometry. Current Protocols in Protein Science. Chapter 12. ss. 12.7.1-12.7.18. doi:10.1002/0471140864.ps1207s43. ISBN 978-0-471-14086-3. PMID 18429296.
- Blow N (Ocak 2009). "Glycobiology: A spoonful of sugar". Nature. 457 (7229). ss. 617-20. Bibcode:2009Natur.457..617B. doi:10.1038/457617a. PMID 19177129.
- Petrie S, Bohme DK (2007). "Ions in space". Mass Spectrometry Reviews. 26 (2). ss. 258-80. Bibcode:2007MSRv...26..258P. doi:10.1002/mas.20114. PMID 17111346.
- Hoffman JH, Chaney RC, Hammack H (Ekim 2008). "Phoenix Mars Mission--the thermal evolved gas analyzer". Journal of the American Society for Mass Spectrometry. 19 (10). ss. 1377-83. doi:10.1016/j.jasms.2008.07.015. PMID 18715800.
- "Cassini Plasma Spectrometer". Southwest Research Institute. 8 Ekim 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Ocak 2008.
Bibliyografi
- Tureček F, McLafferty FW (1993). Interpretation of mass spectra. Sausalito, Calif: University Science Books. ISBN 0-935702-25-3.
- de Hoffman E, Stroobant V (2001). Mass Spectrometry: Principles and Applications. 2nd. John Wiley and Sons. ISBN 0-471-48566-7.
- Downard K (2004). Mass Spectrometry – A Foundation Course. Cambridge UK: Royal Society of Chemistry. ISBN 0-85404-609-7.
- Siuzdak G (1996). Mass spectrometry for biotechnology. Boston: Academic Press. ISBN 0-12-647471-0.
- Dass C (2001). Principles and practice of biological mass spectrometry. New York: John Wiley. ISBN 0-471-33053-1.
- Muzikar P (2003). "Accelerator Mass Spectrometry in Geologic Research". Geological Society of America Bulletin. Cilt 115. ss. 643-654. Bibcode:2003GSAB..115..643M. doi:10.1130/0016-7606(2003)115<0643:AMSIGR>2.0.CO;2. ISSN 0016-7606.
- Maher S, Jjunju FP, Taylor S (2015). "100 years of mass spectrometry: Perspectives and future trends". Rev. Mod. Phys. 87 (1). ss. 113-135. Bibcode:2015RvMP...87..113M. doi:10.1103/RevModPhys.87.113.
- Sobott F (2014). Biological Mass Spectrometry. Boca Raton: Crc Pr I Llc. ISBN 1439895279.
- Sparkman OD (2006). Mass Spectrometry Desk Reference. Pittsburgh: Global View Pub. ISBN 0-9660813-9-0.
- Watson JT, Sparkman OD (2007). Introduction to Mass Spectrometry: Instrumentatio, Applications, and Strategies for Data Interpretation. 4th. Chichester: Jonh Wiley & Sons. ISBN 978-0-470-51634-8.
- Tuniz C (1998). Accelerator mass spectrometry: ultrasensitive analysis for global science. Boca Raton: CRC Press. ISBN 0-8493-4538-3.
- Kandiah M, Urban PL (Haziran 2013). "Advances in ultrasensitive mass spectrometry of organic molecules". Chemical Society Reviews. 42 (12). ss. 5299-322. doi:10.1039/c3cs35389c. PMID 23471277.
Dış bağlantılar
- Curlie'de Mass Spectrometry (DMOZ tabanlı)
- Interactive tutorial on mass spectra Ulusal (ABD) Yüksek Manyetik Alan Laboratuvarı
- Mass spectrometer simulation Bir kütle spektrometrisinin konsolunu simülasyonunu gerçekleştiren interaktif bir uygulama
- Realtime Mass Spectra simulation Tarayıcıda kütle spektrometrisini simüle etmeye yarayan bir araç